Обструктивное апноэ сна и ожирение
Избыточный вес и апноэ сна: когда причина и следствие меняются местами
Даже многие врачи считают, что синдром обструктивного апноэ сна – это проблема исключительно пациентов с ожирением. В какой-то мере такая убежденность имеет под собой почву, потому что избыточный вес действительно является фактором высокого риска для развития нарушений дыхания во время сна. Однако не все здесь так просто и однозначно, как может показаться на первый взгляд непосвященному человеку.
Избыточный вес – фактор риска появления апноэ сна, но эта зависимость работает и в обратную сторону
Ожирение не всегда приводит к апноэ
Остановки дыхания во сне происходят не у всех людей, страдающих ожирением. Последние исследования показали, что на развитие данного заболевания влияет в первую очередь количество жировых отложений в шейной области: чем больше обхват шеи, тем больше сужены дыхательные пути, особенно когда человек находится в положении лежа. И тем легче они могут сомкнуться, создавая тем самым препятствие нормальному току воздуха. Общая масса тела здесь играет второстепенную роль. Чтобы точно оценить риски развития апноэ сна, нужно учитывать не количество подкожного, а количество внутреннего, так висцерального называемого жира.
Косвенными признаками того, что человек с избыточным весом подвержен риску развития ночного апноэ является большие окружность шеи и объем живота на уровне четвертого поясничного позвонка. Поэтому далеко не всегда у людей с ожирением можно выявить апноэ сна, но и не все люди, которые считают, что их вес находится приблизительно в границах нормы, оказываются здоровы.
Апноэ часто само приводит к ожирению
Накапливается все больше доказательств тому, что апноэ сна также влияет на вес человека, причем сугубо отрицательно. Нарушения структуры сна и ночное кислородное голодание, которыми характеризуется данное состояние, приводят к сбоям секреции ряда важных гормонов, участвующего в жировом обмене. В результате избыток калорий активно преобразуется в жир, количество его в организме увеличивается, а вот объем костной и мышечной тканей, наоборот, уменьшается.
Кроме того, свойственная пациентам с обструктивным апноэ сонливость препятствует нормальной физической активности, а малоподвижный образ жизни становится еще одной предпосылкой к набору лишнего веса и трудностям похудания.
Исследователи уже давно отметили взаимосвязь между апноэ сна и ожирением, работающую в обе стороны: лишний вес грозит развитием апноэ, которое, в свою очередь, угрожает прогрессированием ожирения.
А еще бывает и так, что человек, вроде бы не имеющий лишних килограммов, начинает достаточно быстро набирать лишний вес. Если заметное увеличение массы тела сопровождается плохим сном с храпом, повышением артериального давления по утрам, хронической усталостью и сонливостью, нужно обязательно посетить врача-сомнолога и проверить, не связаны ли все указанные симптомы с нарушениями дыхания во сне.
Худеющие тоже плачут
Если человек решился нормализовать собственный вес и с этой целью корректирует свой рацион, здесь тоже могут возникнуть сюрпризы, и достаточно неприятные. Во-первых, несбалансированное питание отрицательно влияет на качество ночного сна и его структуру. А поскольку многие люди любят у нас придумывать себе диеты самостоятельно, причем выбирают наиболее «жесткие» варианты, рассчитывая на максимально быстрый успех, то высок риск, что от такой диеты лишние килограммы не только не уйдут, но потом еще и приумножатся. Низкокалорийные диеты приводят к увеличению времени засыпания и уменьшают продолжительность фазы медленного сна, что неблагоприятно сказывается на состоянии обмена веществ.
Во-вторых, людям, пытающимся сидеть на сверхстрогой диете, присущи так называемые «пищевые срывы», когда, отказывая себе в полноценном питании в течение дня, к вечеру они не выдерживают-таки и съедают таки «запретную вкусняшку». Высокоуглеводная пища перед сном снижает секрецию гормоном сна мелатонина и также заметно ухудшает его качество.
Дневная сонливость и малоподвижный образ жизни увеличивают вес
Все эти факторы в итоге приводят к тому, что вес никуда не девается или вообще увеличивается, сон не улучшается, а даже становится хуже, а апноэ продолжает прогрессировать. Что делать в такой ситуации? Проконсультироваться со специалистами, в первую очередь. И лечить апноэ сна параллельно с нормализацией веса, а не «когда-нибудь потом». И не стоит надеяться, что «вот похудею и остановки дыхания во сне прекратятся сами по себе». И похудеть вряд ли получится, поскольку апноэ мешает процессу снижения веса, и апноэ не прекратятся, потому что вес, не смотря на все ваши усилия, скорее всего если и снизится, то незначительно. Нарушение гормонального фона, приводящее к нарушению баланса между чувством голода и насыщением, процессами жиросжигания и набора веса, постоянная дневная усталость, ведущая к снижению физической активности и серьезные проблемы со стороны сердечно-сосудистой системы просто не позволят вам стать стройнее и почувствовать себя лучше. А ведь апноэ влияет на наш организм именно таким образом.
Ожирение и синдром обструктивного апноэ во сне: как разорвать порочный круг
Существует ли безопасное средство, которое бы одновременно продлевало жизнь, увеличивало энергию, обеспечивало продукцию важных гормонов, улучшало обмен веществ, способствовало метаболизму жира и накоплению мышечной массы, увеличивало концентрацию внимания и улучшало настроение? Простой и эффективный способ достичь этого – хороший ночной сон.
Сон – генетически обусловленная функция организма всех млекопитающих. Если живое существо лишают сна, оно умирает.
Ранее считалось, что сон – пассивный процесс. В настоящее время доказано, что это чрезвычайно сложный процесс, обеспечивающий жизнедеятельность. Отделы мозга, которые днем отвечают за взаимодействие организма с внешней средой, ночью переключаются на настройку органов и систем. В это время суток происходит восстановление иммунитета, регуляция гормонального статуса, очищение органов и систем от токсинов и др.
Следовательно, нарушение сна может приводить к разным изменениям в работе организма, в частности изменению обменных процессов и развитию ожирения. Ожирение в свою очередь является основным фактором риска развития синдрома обструктивного апноэ во сне (СОАС). СОАС усугубляет нарушение сна и обменных процессов, что способствует дальнейшему прогрессированию ожирения. Порочный круг замыкается. Разорвать его в отсутствие эффективного лечения СОАС сложно.
Определение и классификация
Классическое определение заболевания дано в работе C. Guilleminault и соавт. в 1976 г. [1]. Синдром обструктивного апноэ во сне – состояние, характеризующееся храпом, периодическим спадением верхних дыхательных путей на уровне глотки и прекращением легочной вентиляции при сохраняющихся дыхательных усилиях, снижением уровня кислорода в крови, грубой фрагментацией сна и избыточной дневной сонливостью.
В Международной классификации расстройств сна третьего пересмотра приведено более расширенное определение [2]. Так, для постановки диагноза СОАС должны выполняться критерии A и B или только критерий С.
А. Наличие одного критерия или более из следующих:
В. По результатам полисомнографии (ПСГ) или амбулаторного мониторирования (АМ) выявляются:
С. По результатам ПСГ или АМ выявляется 15 или более преимущественно обструктивных респираторных событий (обструктивные или смешанные апноэ, гипопноэ, RERA) за час сна по данным ПСГ или за час наблюдения по данным АМ.
Таким образом, при наличии от пяти до 15 респираторных событий в час диагноз устанавливается только при наличии сопутствующей клинической картины, 15 эпизодов и более – даже в отсутствие клинических проявлений.
Исходя из количества респираторных событий в час (индекс апноэ/гипопноэ – ИАГ), выделяют следующие степени тяжести СОАС:
У пациентов с сахарным диабетом 2 типа распространенность среднетяжелого СОАС (ИАГ ≥ 15) достигает 36% [5]. Учитывая эти данные, а также отрицательное влияние СОАС на функцию бета-клеток и инсулинорезистентность, Международная федерация диабета настоятельно рекомендовала при работе с пациентами с сахарным диабетом 2 типа или синдромом обструктивного апноэ во сне обеспечить надлежащую клиническую практику: при наличии одного из этих заболеваний иметь настороженность в отношении другого [6].
Среди пациентов с гипотиреозом СОАС встречается в 25–60% случаев [7, 8].
Механизмы развития ожирения при синдроме обструктивного апноэ во сне
Пик секреции гормона роста (соматотропина) и тестостерона приходится на глубокие стадии сна [9]. Известно, что при СОАС таковые практически отсутствуют [10].
Дефицит соматотропного гормона у взрослых пациентов с СОАС обусловливает развитие центрального ожирения, уменьшение мышечной и костной массы. Установлено, что при недостаточности соматотропного гормона избыток калорий откладывается не в виде мышечной массы, а в виде жира, который не может быть востребован [11, 12]. При этом как немедикаментозные, так и медикаментозные меры, направленные на снижение массы тела, малорезультативны.
Отложение жира в области шеи приводит к сужению дыхательных путей и прогрессированию СОАС. Как следствие, дефицит соматотропина нарастает. Таким образом, создается порочный круг, разорвать который без специального лечения практически невозможно [10].
Существуют и другие предпосылки для увеличения массы тела у пациентов с СОАС. Значительное деструктурирование сна ассоциируется с увеличением продукции грелина. Данный гормон стимулирует аппетит [13].
При СОАС также отмечается депрессия, дневная сонливость, упадок сил [14], что препятствует увеличению двигательной активности, столь необходимой для борьбы с излишним весом.
Как было отмечено ранее, в данной ситуации чрезвычайно сложно реализовывать программы по модификации образа жизни. Кроме того, такие программы у пациентов с тяжелой степенью СОАС, как правило, неэффективны – масса тела продолжает увеличиваться [15].
С учетом высокой частоты встречаемости СОАС у пациентов эндокринологического профиля необходима настороженность в отношении данной патологии.
На первом этапе можно применять решающее клиническое правило [16]: при наличии трех или более жалоб из пункта 1 или хотя бы одного критерия из пунктов 2 и 3 пациента относят к группе риска развития СОАС (таблица).
Далее для исключения или подтверждения патологии проводят скрининг.
Золотым стандартом диагностики СОАС признана полисомнография – метод длительной регистрации разных параметров работы организма во сне. Это достаточно трудоемкий и дорогостоящий метод, поэтому его применение для диагностики СОАС постепенно сокращается.
В настоящее время минимально достаточными являются респираторный мониторинг и компьютерная сомнография. Данные методы относятся к категории амбулаторных и могут применяться как в условиях стационара, так и в домашних условиях.
Компьютерная сомнография позволяет определить периферический артериальный тонус (Periferal Arterial Tone – PAT-сигнал), частоту сердечных сокращений, сатурацию, дыхательные движения и позицию тела. При этом используются только два датчика. Метод позволяет установить не только апноэ/гипопноэ, но и длительность, структуру сна. Таким образом, с высокой точностью рассчитывается частота апноэ/гипопноэ за час сна. Еще одним преимуществом компьютерной сомнографии считается высокодостоверная автоматическая обработка данных. Результат готов уже через пять минут после сдачи прибора пациентом.
Основной метод лечения СОАС – создание положительного давления в дыхательных путях (ПАП-терапия). Разновидностями ПАП-терапии являются СИПАП- и БИПАП-терапия. В первом случае создается постоянное положительное давление, во втором – двухуровневое положительное давление. Наиболее часто применяется СИПАП-терапия. БИПАП-терапия показана при сочетании СОАС и хронической дыхательной недостаточности на фоне ожирения или патологии легких.
Согласно данным клинической практики, у пациентов, получавших ПАП-терапию, масса тела снижалась легче [10].
Автором статьи также установлено, что диета, физическая нагрузка в сочетании с СИПАП-терапией способствовали достоверному уменьшению массы тела у пациентов с ожирением и СОАС [15].
Единственным препаратом, зарегистрированным для лечения синдрома обструктивного апноэ во сне, является лираглутид (Саксенда). Доказано, что препарат достоверно снижает ИАГ. Очевидно, что этот эффект достигается за счет существенного снижения массы тела [17]. В показаниях для применения данного препарата указано: «В качестве дополнения к низкокалорийной диете и усиленной физической нагрузке для длительного применения с целью коррекции массы тела у взрослых пациентов с ИМТ ≥ 30 кг/м 2 (ожирение) или ≥ 27 кг/м 2 и 2 (избыточная масса тела) при наличии хотя бы одного связанного с избыточной массой тела сопутствующего заболевания/состояния (такого, как предиабет, сахарный диабет 2 типа, артериальная гипертензия, дислипидемия или синдром обструктивного апноэ во сне)».
Бариатрическая хирургия также может рассматриваться в качестве метода лечения пациентов с ожирением и СОАС. В настоящее время бариатрия позиционируется не просто как метод лечения ожирения, а как способ коррекции метаболических нарушений, в частности сахарного диабета 2 типа. В третьем глобальном отчете Международной федерации хирургии ожирения и метаболических расстройств указано, что бариатрические вмешательства позволяют эффективно бороться с сахарным диабетом 2 типа, артериальной гипертензией и СОАС [18].
Необходимо отметить, что бариатрия ассоциируется с определенными рисками. Речь, в частности, идет о рисках во время операции и в послеоперационный период (проблемы с пищеварением, всасываемостью витаминов и микроэлементов). Поэтому бариатрия должна рассматриваться в качестве резервного метода в тех случаях, когда другие методы лечения ожирения не дали результата.
Синдром обструктивного апноэ во сне является частым заболеванием, существенно ухудшающим прогноз у пациентов с ожирением и эндокринной патологией. Знание клинических проявлений заболевания, его патогенетической связи с ожирением, методов диагностики и лечения позволит более эффективно лечить таких пациентов.
Большие проблемы больших людей: дыхательная недостаточность при ожирении и синдроме ночного апноэ
Одышка в той или иной степени знакома практически каждому из нас. Но в норме она возникает лишь при больших перегрузках – физических или эмоциональных. А вот если ощущение нехватки воздуха беспокоит при обычных нагрузках или даже в покое, то пора бить тревогу – это может быть первым признаком серьезных проблем, таких как дыхательная или сердечная недостаточность. Это нередко становится следствием хронического перенапряжении сердечной и дыхательной систем при значительном избыточном весе. А ожирение, как вы помните, еще и фактор риска появления остановок дыхания во сне.
Избыточный вес – это, в первую очередь, огромная нагрузка на организм, от которой больше всего страдают сердечно-сосудистая и дыхательная системы
Когда лишний вес достигает «критического» для человека значения, он теряет способность дышать достаточно глубоко, что приводит к так называемой гиповентиляции: когда грудная клетка оказывается в капкане из жировых отложений и легкие утрачивают способность полноценно наполнятся воздухом. В результате в мельчайших структурах легочной ткани нарушается обмен кислорода и углекислого газа. При этом содержание кислорода в крови снижается, а насыщенность крови углекислым газом, напротив, возрастает. Кроме того, дыхательная система, вынужденная работать в предельно интенсивном режиме в течение дня, переутомляется от такой постоянной перегрузки, поэтому во время ночного сна, когда часть мышцы естественным образом расслабляется, нарушения дыхания еще большее усугубляются. А так как большая часть таких людей одновременно имеет еще и синдром обструктивного апноэ сна, то дыхательная недостаточность у них после засыпания резко прогрессирует. Это состояние получило название синдрома ожирения-гиповентиляции или синдрома Пиквика. При отсутствии своевременного лечения пиквикский синдром приводит к сердечной недостаточности, инвалидности и преждевременной смерти.
Проявления синдрома Пиквика включают:
Если у вас или знакомых вам людей кроме храпа и лишнего веса присутствует хотя бы еще один дополнительный симптом из этого списка, то нужно обязательно проконсультироваться с врачом.
Вспомогательная вентиляция легких как метод лечения синдрома Пиквика
Сегодня лечение людей с синдромом ожирения-гиповентиляции представляет серьезную медицинскую проблему: эффективных таблеток нет и пока не предвидится, снижение веса – долгосрочная перспектива, тогда как здоровье ухудшается с каждым днем, а кислородотерапия у таких больных не дает должного эффекта при лечении их дыхательной недостаточности – ведь основная проблема таких пациентов заключается в неспособности полноценно дышать. Наличие остановок дыхания требует обязательного лечения апноэ сна, но одного этого часто бывает недостаточно. И все же способ, позволяющий эффективно восстановить дыхательную функцию, вылечить апноэ сна и предотвратить фатальные осложнения гиповентиляции на фоне ожирения, существует.
Это вспомогательная вентиляция легких через закрывающую нос и рот пациента маску – так называемая БиПАП-терапия. Так как наиболее тяжелая дыхательная недостаточность развивается у пациентов с пиквикским синдромом во время сна, то и лечение обычно проводится ночью. В отличие от аппарата СиПАП такой прибор обеспечивает не один, а два разных уровня положительного давления воздуха. Меньшее давление на выдохе, как и СиПАП поддерживает верхние дыхательные пути открытыми во время сна, а большее давление вдоха позволяет наполнить легкие пациента достаточным количеством воздуха – обеспечить поступление должного количества кислорода и удалить углекислый газ. Отдохнувшая за ночь система дыхания после этого оказывается способной поддерживать адекватный газообмен в течение дня.
Случай из клинической практики
К нам обратилась пациентка – женщина 52-х лет, по профессии бухгалтер. В возрасте 37 лет – после вторых родов – набрала около 40 килограммов. Вскоре она стала замечать, что повседневные дела даются со все большим и большим трудом, при подъеме по лестнице, а затем и просто при спокойной ходьбе стала появляться одышка. Затем дышать и вовсе стало физически тяжело, особенно лежа на спине, поэтому она могла спать только на боку. Муж заметил, что супруга стала во сне громко храпеть и, по косвенным признакам, описывал у нее обструктивное апноэ сна. Сама пациентка жаловалась на сон с частыми пробуждениями, разбитость и выраженную сонливость днем. Она стала с трудом справляться с работой. Из-за практически постоянно повышенного артериального давления то и дело возникали сильные головные боли. Когда женщина обратилась за помощью, ее дыхание было частым и поверхностным, губы имели синеватый оттенок, на ногах отчетливо видны были отеки. При первом осмотре артериальное давление было 210/110 мм рт. ст., сердцебиение учащенное и неритмичное. Со слов пациентки, лекарства для понижения давления помогали ей последнее время все хуже. Дополнительные обследования выявили признаки сахарного диабета и расширение камер сердца на фоне снижения его тонуса.
Для выявления тяжести дыхательной недостаточности и выявления причины храпа мы провели исследование дыхательной функции пациентки, содержание газов в крови и респираторное мониторирование во время сна. Результат получился удручающим: была диагностирована хроническая дыхательная недостаточность, а количество остановок дыхания во сне было составил 93 в час. При этом даже в редкие периоды, когда обструктивные апноэ отсутствовали показатели насыщения крови кислородом оставались крайне низкими, что было явным признаком гиповентиляции.
Помочь пациентке могла только неинвазивная вентиляция легких. В начале было необходимо устранить остановки дыхания во сне – обструктивные апноэ. Для этого ей была назначена СиПАП терапия, которая дала возможность пациентке свободно дышать по ночам, но альвеолярную гиповентиляцию скорректировала лишь частично, повысив, но не нормализовав содержание кислорода в крови. Поэтому продолжена терапия была при помощи аппарата БиПАП. Назначенный курс лечения сочетался с лекарственной терапией, направленной на нормализацию цифр артериального давления.
Явный положительные результат был отмечен уже через неделю лечения: нормализовался сон и прошла изнуряющая дневная сонливость, частота дыхания и состав газов крови приблизились к нормальным, существенно уменьшилась одышка и возросла переносимость физических нагрузок. Показатели артериального давления стабилизировались в пределах возрастной нормы. Таким образом, на фоне восстановления дыхательной функции были побеждены синдром ожирения-гиповентиляции и синдром ночного апноэ.
Данный клинический случай наглядно иллюстрирует, что СиПАП терапия восстанавливает проходимость дыхательных путей во время ночного сна и гарантированно предотвращает апноэ, а БиПАП терапия устраняет еще и явления гиповентиляции – дыхательной недостаточности. Правильный подбор вспомогательной вентиляции позволяет эффективно лечить пациентов, страдающих от дыхательной недостаточности и апноэ сна на фоне ожирения.
Синдром обструктивного апноэ сна и ожирение у детей: точки соприкосновения
Опубликовано в журнале:
Практика педиатра, сентябрь-октябрь, 2017
Ключевые слова: сон, ожирение у детей, синдром обструктивного апноэ сна у детей
Keywords: sleep, obesity in children, obstructive sleep apnea syndrome in children
Одной из глобальных проблем современности является неуклонный рост распространенности ожирения. Особую обеспокоенность вызывает рост ожирения в детском возрасте. Так, по данным Всемирной организации здравоохранения, 41 млн детей в возрасте до 5 лет страдают избыточным весом или ожирением. Большая часть населения планеты проживает в странах, где от последствий избыточного веса и ожирения умирает больше людей, чем от последствий аномально низкой массы тела [1]. Хорошо известно, что избыточный вес и ожирение у детей и подростков, а также сопутствующие им заболевания, представляют серьезную угрозу состоянию здоровья ребенка. В литературе широко описаны заболевания, сопутствующие ожирению: сердечно-сосудистые, эндокринологические, неврологические, легочные, ортопедические, патология желудочно-кишечного тракта и психосоциальная патологии [2].
Одной из недостаточно изученных у детей патологией, связанной с ожирением, является синдром обструктивного апноэ сна (СОАС), который входит в раздел нарушений дыхания во сне [3]. Известно, что у взрослого населения ожирение – наиболее значимый фактор, предрасполагающий к развитию обструкции дыхательных путей [4]. В детской популяции 60% детей с ожирением имеют осложнение в виде СОАС [5].
Необходимо отметить, что имеются данные о взаимосвязи между продолжительностью и качеством сна и риском развития ожирения [6] (рис. 1).
Рис. 1. Взаимосвязь СОАС и ожирения
Таким образом, нарушения сна, в частности СОАС, и ожирение являются взаимодополняющими проблемами и требуют комплексного подхода к их решению (таблица).
Точки соприкосновения СОАС и ожирения
| Показатель | Ожирение | СОАС |
| 1. Сердечно-сосудистая патология | ||
| гиперлипидемия | + | |
| повышенный уровень кровяного давления | + | + |
| сосудистая дистония | + | + |
| ранний коронарный и аортальный атеросклероз | + | |
| расширение и дисфункция левого желудочка и предсердия | + | + |
| 2. Эндокринная патология | ||
| метаболический синдром | + | + |
| гиперинсулинемия | + | + |
| инсулинорезистентность | + | + |
| предиабет | + | + |
| сахарный диабет 2-го типа | + | + |
| 3. Психосоциальная патология | ||
| психологическое расстройство по поводу собственного внешнего вида | + | |
| низкая самооценка | + | + |
| нарушенная социализация | + | + |
| виктимизация | + | |
| депрессивные симптомы | + | + |
| беспорядочное питание | + | + |
| тревожность | + | + |
Основные угрожающие последствия СОАС у детей связаны с нейробиологическими, сердечно-сосудистыми, эндокринными и метаболическими нарушениями. Синдром обструктивного апноэ во сне проявляется у детей длительной регулярной или приходящей полной обструкцией верхних дыхательных путей, что приводит к периодической гипоксемии, гиперкапнии с последующим пробуждением и фрагментации сна [7, 8]. Это клиническое нарушение, характеризующееся частыми остановками дыхания во время сна, обычно они сопровождаются громким храпом. СОАС в детском возрасте может появиться в любое время, но пик встречаемости приходится на период от 2 до 6 лет, что совпадает с максимальным разрастанием небных миндалин, которые перекрывают дыхательные пути на уровне глотки [9]. Помимо гипертрофии небных миндалин, СОАС могут вызывать структурные аномалии верхних дыхательных путей, возникшие в результате снижения тонуса мышечной стенки ВДП или дискоординации работы дыхательной мускулатуры и потока воздуха, а также наличие ожирения.
Выделяют дневные и ночные клинические симптомы СОАС. Основным ночным симптомом СОАС является храп. Помимо этого, у ребенка отмечается дыхание ртом, усиление дыхания при физической нагрузке или затруднение дыхания во сне, появление эпизодов обструкции, усиленное потоотделение во сне, беспокойство и частые ночные пробуждения, непривычная поза во сне и жалобы родителей на дыхание ребенка ночью [10, 11]. К дневным симптомам СОАС относятся: увеличение потребности в дневном сне, гиперактивное поведение, трудности в обучении и когнитивные нарушения [12, 13].
Диагностическим критерием СОАС у детей считается индекс апноэ-гипопноэ (ИАГ) > 5 в час сна (по данным полисонмографии) и присутствие симптомов чрезмерной дневной сонливости [14]. СОАС, по разным данным, охватывает 2–3% детей [15]. Однако у детей, страдающих ожирением, его распространенность достигает 59% [16]. У детей с СОАС и ожирением значительно увеличивается риск кардиоваскулярной патологии. По данным клинических исследований, СОАС связан с такими факторами риска развития сердечнососудистых заболеваний, как эндотелиальная дисфункция, артериальная гипертензия, аритмии и сердечная недостаточность [17–20].
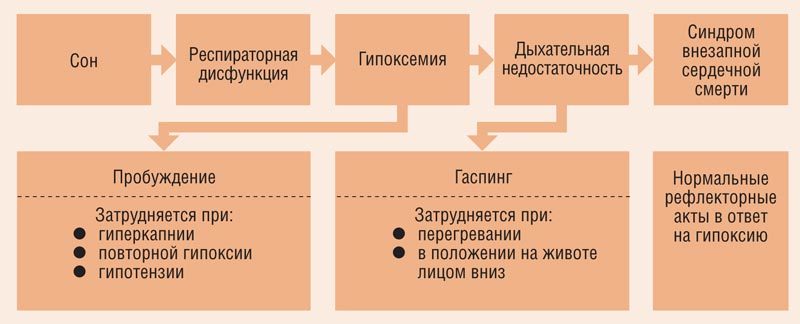
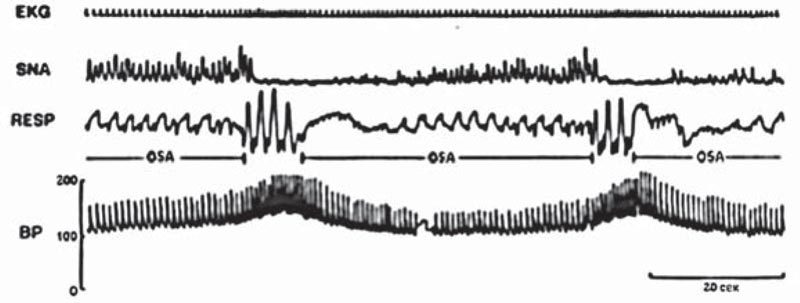
Ключом к пониманию гемодинамических реакций на синдром обструктивного апноэ сна является концепция так называемого «дайвинг-рефлекса». Он состоит в следующем: апноэ вызывает гипоксемию, которая стимулирует парасимпатическую активность и приводит к брадикардии; повышенная периферическая симпатическая активность сужает периферические сосуды и повышает артериальную резистентность. Типичный эпизод обструкции во сне может приводить к брадикардии (или даже к кратковременной остановке синусового узла) и постепенно увеличивать периферическую симпатическую нейронную активность. Когда обструкция купируется, симпатическая нейронная активность достигает своего максимума, что резко увеличивает кровяное давление и сердечный ритм, это увеличение совпадает с компенсаторным гиперпноэ [21–23] (рис. 2, 3).
Рис. 2. Нарушение дыхательных функций (Adrian Walker, 1996)
Рис. 3. Записи во время сна у пациентов с СОАС
Эпизоды обструкции верхних дыхательных путей во время сна у пациентов с СОАС вызывают увеличение внутригрудного давления, выброс адреналина и вторичную дисфункцию эндотелия. Также одну из ключевых ролей играет возникновение оксидантного стресса на фоне эпизодов гипоксии. Ожирение и СОАС являются заболеваниями, сопровождающимися системным воспалением [24–26]. В крови у детей с СОАС обнаружено повышение провоспалительных цитокинов, таких как интерлейкин-6, а также С-реактивный белок [27]. Однако многие из этих факторов также тесно связаны с ожирением, поэтому исследования направлены на выявление того, являются ли такие ассоциации независимыми от ожирения. В поддержку независимого влияния СОАС представлены данные когортного исследования здоровых подростков, которые демонстрируют прогрессирующее повышение уровней СРБ, что указывает на то, что даже умеренные проявления СОАС при отсутствии сопутствующей патологии могут приводить к повышению воспалительных маркеров [28].
Другим механизмом развития сердечнососудистых осложнений является повышение тонуса симпатической нервной системы. Исследования показали наличие существенных изменений симпатического тонуса у детей с СОАС [29]. Острая симпатическая активация, связанная с апноэ во время сна, и устойчивое повышение симпатической активности при пробуждении играет критически важную роль в генерации сердечных аритмий у пациентов с синдромом удлиненного интервала QT [30]. В исследованиях была подтверждена связь между СОАС и развитием аритмии [31]. Наиболее распространенными аритмиями во время сна являются неосложненная желудочковая тахикардия, пауза/остановка синусового узла, атриовентрикулярная блокада второй степени и преждевременное сокращение желудочков (ПВХ > 2 уд./ мин) [32, 33].
Продолжают изучаться патофизиологические связи между фибрилляцией предсердий и апноэ во сне. Вероятно, фибрилляция предсердий при СОАС связана с наличием ожирения, расширением предсердий, гипертонией и вегетативным дисбалансом. В ряде работ сообщалось об увеличении размера предсердий среди пациентов с СОАС [34, 35]. СОАС приводит к изменениям активности сердечных ганглиозных сплетений, что, по-видимому, влияет на период рефрактерности предсердий [36].
Еще одним угрожающим последствием СОАС у детей с ожирением является повышенный риск развития внезапной сердечной смерти. Так, в некоторых работах было продемонстрировано, что у детей с частыми проявлениями СОАС значительно повышался риск внезапной сердечной смерти по сравнению с контрольной группой [37]. В когорте детей с ожирением итак повышен риск развития вышеперечисленных заболеваний, СОАС же вносит дополнительный вклад в развитие данных патологий, замыкая «порочный круг». Именно поэтому оценка наличия эпизодов обструкции во сне является обязательным звеном в ведении пациентов с морбидным ожирением.
Имеются данные, свидетельствующие о том, что ночные пробуждения связаны с изменениями активности гипоталамо-гипофизарно-надпочечниковой системы и увеличением пульсирующего выброса кортизола [38]. Повышенный уровень кортизола связан с многочисленными неблагоприятными последствиями, такими как метаболический синдром, диабет, гипертония, депрессия и бессонница [39]. В некоторых популяционных исследованиях отмечено, что распространенность метаболического синдрома среди детей составляет 3,3% у детей без ожирения, 11,9% у детей с избыточной массой тела, а у детей с ожирением 29,2% [40].
Известно также, что повышенные уровни кортизола вызывают снижение секреции гормона роста [41]. В литературе описано, что у детей с обструкцией верхних дыхательных путей обнаруживаются дефекты роста из-за снижения секреции гормона роста. Секреция данного гормона восстанавливается после аденотозиллэлектомии [42].
Данные различных исследований свидетельствуют о том, что как СОАС, так и ожирение приводят к значительному снижению качества жизни детей, особенно когда имеет место наличие обеих патологий [43, 44]. Качество жизни улучшается после лечения СОАС [43].
Известно, что у детей, страдающих ожирением, в 1,8 раза чаще, чем у детей с нормальным весом, отмечается низкая само-оценка [45]. Многие исследования показали наличие четкой ассоциации между СОАС и синдромом дефицита внимания с гиперактивностью, и другими поведенческими нарушениями [46– 49]. Механизм возникновения этих симптомов заключается в нарушении сна и возникновении эпизодов гипоксии. Это приводит к нарушению таких функции префронтальных областей коры головного мозга, как рабочая память, поведенческий контроль, анализ, организация, саморегуляция [50, 51].
Практикующие врачи, к сожалению, не всегда уделяют должное внимание обследованию детей на предмет выявления у них СОАС. Однако важно помнить, что диагностика СОАС у детей основана на клиническом обследовании и полисомнографии [52]. Клиническое обследование необходимо для более точной интерпретации полисомнографических данных, выявления сопутствующей и основной патологии и исключения причин нарушения дыхания, не связанных с обструктивным апноэ сна. При клиническом обследовании пациентов с СОАС возможно обнаружение следующих симптомов: ретрогнатия, арочное нёбо, гипертрофия небных миндалин.
Американская академия педиатрии рекомендует полисомнографию в качестве диагностического теста для детей с подозрением на СОАС [53]. Полисомнография представляет собой синхронную запись различных физиологических параметров во время сна. Протокол исследования с целью диагностики нарушений сна включает проведение электроэнцефалограммы, электроокулограммы, электромиограммы, электрокардиограммы, оценку респираторной активности, показателей насыщения крови кислородом, артериального давления, частоты сердечных сокращений, двигательной активности грудной клетки и передней брюшной стенки, ортоназального потока воздуха, шума дыхания, положения тела в постели и движения конечностей во сне [54].
Методы лечения СОАС у детей включают: аденостонзилотомию, применение назальной маски для создания положительного давления в дыхательных путях во время сна (CPAP-терапия), ротовых аппликаторов, назначение противовоспалительных препаратов. Аденостонзиллотомия назначается в 83% случаев и является первоочередным методом лечения у детей, страдающих СОАС. В послеоперационном периоде необходимо клиническое наблюдение, так как в 15–20% выявляются остаточные явления [55]. Риск развития послеоперационных осложнений выше у детей младше 3 лет, детей страдающих СОАС, ожирением и другой сопутствующей патологией [56]. Соответственно, необходимо проводить повторные исследования сна в ночное время после аденотонзиллотомии.
CPAP-терапия применима у детей с хроническим СОАС после проведенной аденотонзилотомии или с противопоказаниями к хирургическому лечению [57]. CPAP-терапия – полностью безопасный метод лечения, но требует времени для привыкания и обучения родителей.
Список литературы:
1. Информационный бюллетень ВОЗ. 2016. Июнь.2. Grant-Guimaraes, Jamilah et al. Childhood Overweight and Obesity Gastroenterology Clinics // Gastroenterology Clinics Vol. 45. Issue 4. P. 715–728.3. Brouilette R., Hanson D., David R. et al. A diagnostic approach to suspected obstructive sleep apnea in children // J. Pediatr. 1984. Vol. 105. Р. 10–4
4. Вейн А.М., Елигулашвили Т.С., Полуэктов М.Г. Синдром апноэ во сне. М.: Эйдос-Медиа, 2002.
12. Mindel J.A., J.A.Owens. A Clinical guide to Pediatric Sleep: Diagnosis and Management of Sleep Problems; 2nd ed. Philadelphia, USA: LIPPICOTT WILLIAMS &WILKINS, 2010.
13. Mindell J.A., L.S. Telofski, B. Wiegand, E.S. Kurtz. A Nightly Bedtime Routine: Impact on Sleep in Young Children and Maternal Mood // Sleep. 2009. Vol. 32, № 5. Р. 599–606.
14. Jambhekar S, Carroll JL. Diagnosis of pediatric obstructive sleep disordered breathing: Beyond the gold standard // Expert Rev Respir Med. 2008; 2:791–809/15. Marcus CL. Sleep-disordered breathing in children // Am J Respir Crit Care Med. 2001; 164: 16–30.16. Verhulst SL, Van Gaal L, De Backer W. et al. The prevalence, anatomical correlates and treatment ofsleep-disordered breathing in obese children and adolescents // Sleep Med Rev 2008; 12: 339–346.
17. Gozal D, Kheirandish-Gozal L. Childhood obesity and sleep: relatives, partners, or both? // Ann NY Acad Sci. 2012; 1264: 135–141.
18. Bhattacharjee R, Kheirandish-Gozal L, Pillar G, Gozal D. Cardiovascular omplications of obstructive sleep apnea syndrome: evidence from children // Prog Cardiovasc Dis. 2009; 51: 416–433.
19. Kheirandish-Gozal L, Bhattacharjee R, Gozal D. Autonomic alterations and endothelial dysfunction in pediatric obstructive sleep apnea // Sleep Med. 2010; 11: 714–720.
20. Bhattacharjee R, Kim J, Alotaibi WH, Kheirandish-Gozal L, Capdevila OS, Gozal D. Endothelial dysfunction in children without hypertension: potential contributions of obesity and obstructive sleep apnea // Chest. 2012; 141: 682–691.
21. Somers VK, Dyken ME, Clary MP, Abboud FM. Sympathetic neural mechanisms in obstructive sleep apnea // J Clin Invest 1995; 96(4): 1897–904.
22. Somers VK, Dyken ME, Mark AL, Abboud FM. Parasympathetic hyperresponsiveness and bradyarrhythmias during apnoea in hypertension // Clin Auton Res. 1992; 2(3): 171–6.
23. Sabharwal R, Zhang Z, Lu Y, Abboud FM, Russo AF, Chapleau MW. Receptor activity-modifying protein 1 increases baroreflex sensitivity and attenuates angiotensin-induced hypertension // Hypertension 2010; 55(3): 627–35.
24. Zaldivar F, McMurray RG, Nemet D, Galassetti P, Mills PJ, Cooper DM. Body fat and circulating leukocytes in children // J Obes (Lond) 2006; 30: 906–911.
25. Cindik N, Baskin E, Agras PI et al. Effect of obesity on inflammatory markers and renal functions // Acta Paediatr 2005; 94: 1732–1737.
26. Gozal D, Kheirandish L. Oxidant stress and inflammation in the snoring child: confluent pathways to upper airway pathogenesis and end-organ morbidity // Sleep Med Rev.2006;10: 83–96.
27. Gozal D, Serpero LD, Sans Capdevila O, Kheirandish-Gozal L. Systemic inflammation in non-obese children with obstructive sleep apnea // Sleep Med 2008; 9: 254–9.
28. Larkin EK, Rosen CL, Kirchner HL et al. Variation of C-reactive protein levels in adolescents: association with sleep-disordered breathing and sleep duration // Circulation. 2005; 111: 1978–84.
29. O’Brien L. M., Gozal D. (2005). Autonomic dysfunction in children with sleep-disordered breathing. Sleep 28, 747–752, O’Brien L. M., Gozal D. (2005). Autonomic dysfunction in children with sleep-disordered breathing. Sleep 28, 747–752, O’Brien L. M., Gozal D. (2005). Autonomic dysfunction in children with sleep-disordered breathing. Sleep 28, 747–752.
30. Antzelevitch C. Sympathetic modulation of the long QT syndrome // Eur Heart J. 2002; 23:1246.
31. Gula LJ, Krahn AD, Skanes A, Ferguson KA, George C, Yee R, et al. Heart rate variability in obstructive sleep apnea: A prospective study and frequency domain analysis // Ann Noninvasive Electrocardiol. 2003; 8: 144–9.
32. Hoffstein V, Mateika S. Cardiac arrhythmias, snoring and sleep apnea // Chest. 1994; 106: 466–71.
33. Koehler U, Schafer H. Is obstructive sleep apnea (OSA) a risk factor for myocardial infarction and cardiac arrhythmias in patients with coronary heart disease (CHD) // Sleep. 1996; 19: 283–6.
34. Orban M, Bruce CJ, Pressman GS et al. Dynamic changes of left ventricular performance and left atrial volume induced by the Mueller maneuver in healthy young adults and implications for obstructive sleep apnea, atrial fibrillation, and heart failure // J Cardiol. 2008; 102(11): 1557–61.
35. Otto ME, Belohlavek M, Khandheria B et al. Comparison of right and left ventricular function in obese and nonobese men // J Cardiol 2004; 93(12): 1569–72.
36. Hou Y, Scherlag BJ, Lin Jet al. Ganglionated plexi modulate extrinsic cardiac autonomic nerve input: effects on sinus rate, atrioventricular conduction, refractoriness, and inducibility of atrial fibrillation // J Am Coll Cardiol 2007; 50(1): 61–8.
37. Kahn A, Groswasser J, Rebuffat E et al. Sleep and cardiorespiratory characteristics of infant victims of sudden death: a prospective case–control study // Sleep.1992; 15: 287–292.
40. Friend A, Craig L, Turner S. The prevalence of metabolic syndrome in children: a systematic review of the literature // Metab Syndr Relat Disord. 2013; 11(2): 71–80.
42. Peltomki T. The effect of mode of breathing on craniofacial growth–revisited // Eur J Orthod. 2007. 29: 426–42943. Franco RA Jr, Rosenfeld RM, Rao M. First place–resident clinical science award 1999: quality of life for children with obstructive sleep apnea // Otolaryngol Head Neck Surg. 2000; 123: 9–16113115.
44. Friedlander SL, Larkin EK, Rosen CL, Palermo TM, Redline S. Decreased quality of life associated with obesity in school-aged children // Arch Pediatr Adolesc Med. 2003; 157: 1206–1211.
45. Chervin RD, Dillon JE, Bassetti C, Ganoczy DA, Pituch KJ. Symptoms of sleep disorders, inattention, and hyperactivity in children // Sleep. 1997; 20: 1185–92.
46. Small L, Aplasca A. Child obesity and mental health: a complex interaction // Child Adolesc Psychiatr Clin N Am 2016; 25(2): 269–82.
47. Owens J, Spirito A, Marcotte A, McGuinn M, Berkelhammer L. Neuropsychological and behavioral correlates of obstructive sleep apnea syndrome in children: A preliminary study // Sleep Breath. 2000; 4: 67–78.
48. Chervin RD, Archbold KH, Dillon JE et al. Inattention, hyperactivity, and symptoms of sleep-disordered breathing // Pediatrics 2002; 109: 449–56.
49. Gottlieb DJ, Vezina RM, Chase C et al. Symptoms of sleep-disordered breathing in 5-year-old children are associated with sleepiness and problem behaviors // Pediatrics. 2003; 112: 870.
50. Chervin RD, Dillon JE, Bassetti C, Ganoczy DA, Pituch KJ. Symptoms of sleep disorders, inattention, and hyperactivity in children // Sleep. 1997; 20: 1185–92.
51. Beebe DW, Gozal D. Obstructive sleep apnea and the prefrontal cortex: towards a comprehensive model linking nocturnal upper airway obstruction to daytime cognitive and behavioral deficits // J Sleep Res 2002; 11: 1–16.
52. Leach J., Olson J., Hermann J., Manning S. Polysomnographic and clinical findings in children with obstructive sleep apnea // Arch. Otolaryngol. Head Neck Surg. 1992. Vol. 118. Р. 741–4.
53. American Academy of Pediatrics. Clinical practice guideline: diagnosis and management of childhood obstructive sleep apnea syndrome // Pediatrics. 2002; 109(4): 704–712.
54. Iber C, ed. The AASM Manual for the Scoring of Sleep and Associated Events: Rules, Terminology and Technical Specification. American Academy of Sleep Medicine; 2007. Ref Type: Serial (Book, Monograph).
55. Brietzke S.E., Katz E.S., Roberson D.W. Can history and physical examination reliably diagnose pediatric obstructive sleep apnea/hypopnea syndrome? A systematic review of the literature // Otolaryngol. Head Neck Surg. 2004. Vol. 131. Р. 827–32.
56. Sanders J.C., King M.A., Mitchell R.B., Kelly J.P. Perioperative complications of adenotonsillectomy in children with obstructive sleep apnea syndrome // Anesth. Analg. 2006. Vol. 103. Р. 1115–21.
57. Massa F, Gonsalez S, Laverty A, Wallis C, Lane R. The use of nasal continuous positive airway pressure to treat obstructive sleep apnoea // Arch Dis Child. 2002; 87: 438–443.