ноздрин с какого возраста детям можно
Опыт применения комбинированных препаратов при лечении ринитов и синуситов у детей
Заболеваемость синуситами до настоящего времени достаточно высока. По данным различных авторов, заболеваниями носа и околоносовых пазух страдает от 17 до 22% детского населения. Одним из существенных факторов патогенеза острых
Заболеваемость синуситами до настоящего времени достаточно высока. По данным различных авторов, заболеваниями носа и околоносовых пазух страдает от 17 до 22% детского населения. Одним из существенных факторов патогенеза острых и особенно хронических воспалительных заболеваний носа и околоносовых пазух является нарушение механизма мукоцилиарного транспорта. Это чаще всего связано с отеком слизистой оболочки, избыточным образованием и повышением вязкости носового секрета, что влечет за собой расстройство дренажной, дыхательной, секреторной и обонятельной функций. Наиболее распространенный метод лечения синуситов — пероральное или внутримышечное назначение антибиотиков. Так как поступление антибиотика из кровяного русла в очаг воспаления ограничено, лечение синуситов должно носить комплексный характер.
В первую очередь это должно касаться улучшения вентиляции, а также дренажа околоносовых пазух и носоглотки.
До настоящего времени врачи-оториноларингологи не всегда практикуют назначение включенных в схему терапии больных синуситами адекватных мукорегулирующих препаратов, которые, разжижая густой вязкий секрет и улучшая мукоцилиарный клиренс, способствуют удалению секрета из пазух. Среди препаратов, воздействующих на мукоцилиарную активность, ранее использовались средства, стимулирующие разжижение ринобронхиального секрета, или так называемые муколитики, которые изменяют вязкость секрета, воздействуя на его физико-химические свойства. Речь идет о ферментах (трипсине, химотрипсине и т. д.), которые из-за наличия побочных эффектов в настоящее время не применяются.
Муколитическим действием обладают также препараты, снижающие поверхностное натяжение, т. е. воздействующие на гель-фазу отделяемого и разжижающие как мокроту, так и носоглоточный секрет. К этой группе относится флуимуцил (N-ацетилцистеин), действие которого связано со способностью свободной сульфгидрильной группы N-ацетилцистеина расщеплять межмолекулярные дисульфидные связи агрегатов гликопротеинов слизи, оказывая сильное разжижающее действие и уменьшая вязкость в отношении любого вида секрета: гнойного, слизисто-гнойного, слизистого. Особенность флуимуцила состоит в том, что помимо прямого муколитического действия N-ацетилцистеин обладает мощными антиоксидантными свойствами и способен обеспечить защиту органов дыхания от цитотоксического воздействия метаболитов воспаления, факторов окружающей среды, табачного дыма.
В группе муколитиков большой интерес представляют комбинированные препараты, а именно ринофлуимуцил, в состав которого кроме N-ацетилцистеина, разжижающего секрет, входит симпатомиметик — туаминогептана сульфат, обладающий мягким сосудосуживающим действием и не вызывающий излишней сухости слизистой оболочки. После разрыва дисульфидных мостиков слизь и мокрота теряют вязкость, начинают впитывать в себя воду и мягко удаляются при сморкании, чихании, кашле. Показаниями к применению ринофлуимуцила являются:
Оценка эффективности препарата производилась в группе из 55 пациентов в возрасте от 6 до 14 лет; ринофлуимуцил впрыскивали по одной дозе в каждую половину носа 3-4 раза в день, курс составил 6-7 дней. Состояние детей оценивали по их субъективным ощущениям до и после применения препарата, а также объективным критериям (уменьшение гиперемии и застойных явлений в слизистой оболочке, улучшение носового дыхания, уменьшение слизи, изменение ее реологических свойств).
Уже после 6-8 ингаляций ринофлуимуцила была отмечена положительная динамика.
Результат применения препарата оценивался следующим образом: 70% больных — отлично; 20% — хорошо; 10% — удовлетворительно.
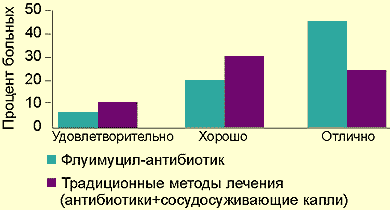 |
| Рисунок. Сравнительные результаты лечения флуимуцилом-антибиотиком ИТ и традиционными методами |
Побочных явлений от применения препарата не отмечено. Достоинство ринофлуимуцила в том, что он воздействует на поверхность слизистой оболочки и, разжижая слизь, уменьшает ее вязкость и способствует продуктивному физиологическому акту очищения полости носа.
Следующий препарат, на который следует обратить внимание, — это флуимуцил-антибиотик ИТ, соединяющий в одной лекарственной форме два компонента: N-ацетилцистеин и тиамфеникола глицинат (тиамфеникол — препарат из группы хлорамфениколов). Спектр антимикробной активности препарата представлен в табл. 1 (Клиническая фармакология антибактериальных препаратов/Под ред. Ю. Б. Белоусова, 1988).
Препарат обладает сочетанным антибактериальным и муколитическим действием и рекомендуется для лечения заболеваний органов дыхания, вызванных бактериальной инфекцией и сопровождающихся образованием густого вязкого секрета. Антимикробная активность тиамфеникола обусловлена его вмешательством в синтез бактериальных белков. Последние исследования показали, что сочетание тиамфеникола и N-ацетилцистеина позволяет препарату сохранять неконъюгированную форму и достигать очага воспаления в концентрациях, достаточных для создания бактерицидного эффекта. Препарат проявляет муколитическую активность в отношении любого вида секрета — слизистого, слизисто-гнойного, гнойного. Флуимуцил-антибиотик ИТ облегчает отделение мокроты и носовой слизи. Препарат эффективен при введении в околоносовые пазухи.
Мы располагаем данными лечения препаратом флуимуцил-антибиотик ИТ у 37 детей, из них у 17 был диагностирован острый гайморит, у 10 — обострение хронического гайморита и у 10 — обострение хронического гнойного гаймороэтмоидита. Контрольная группа пациентов лечилась традиционным методом без применения флуимуцила-антибиотика. Сравнительные данные представлены на рисунке.
Препарат использовался для промывания околоносовых пазух после пункций или после оперативного вмешательства, в том числе после эндоназального вскрытия клеток решетчатого лабиринта. Хорошие результаты были получены уже после 2-3 промываний: улучшилось носовое дыхание, сократился отек слизистой оболочки полости носа, уменьшилось количество секрета, исчез его гнойный характер. Показания и способы применения препарата представлены в табл. 2.
Эффективность флуимуцила-антибиотика ИТ определяется не только антибактериальным воздействием, но и способностью обеспечивать быстрое и полное удаление экссудата, что в свою очередь усиливает антибактериальный эффект.
Литература
Обратите внимание!
Флуимуцил-антибиотик ИТ обладает следующими фармакологическими и терапевтическими свойствами:
Деринат : инструкция по применению
Состав
Описание
Прозрачная бесцветная жидкость без посторонних включений.
Фармакологическое действие
Препарат активирует клеточный и гуморальный иммунитет. Оптимизирует специфические реакции против грибковой, вирусной и бактериальной инфекции. Препарат стимулирует репаративные и регенераторные процессы, нормализует состояние тканей и органов при дистрофиях сосудистого происхождения. Деринат способствует заживлению трофических язв различной этиологии. Деринат способствует быстрому заживлению глубоких ожогов, значительно ускоряя динамику эпителизации. При восстановлении язвенных образований на слизистой под действием Дерината происходит безрубцовое восстановление. Препарат не обладает тератогенным и канцерогенным действиями.
Фармакокинетика
Показания к применению
— острые респираторные заболевания (ОРЗ):
— профилактика и лечение острых респираторных вирусных инфекций (ОРВИ);
— офтальмология: воспалительные и дистрофические процессы;
— воспалительные заболевания слизистых оболочек полости рта;
— хронические воспалительные заболевания, грибковые, бактериальные и другие инфекции слизистых в гинекологии;
— острые и хронические заболевания верхних дыхательных путей (ринит, синусит, гайморит, фронтит);
— трофические язвы, длительно незаживающие и инфицированные раны (в том числе при сахарном диабете);
— постлучевые некрозы кожи и слизистых.
Противопоказания
Беременность и период лактации
Способ применения и дозы
При заболеваниях слизистой полости рта производят полоскание препаратом 4-6 раз в сутки (1 флакон 1-2 полоскание). Продолжительность курса лечения 5-10 дней.
Побочное действие
При гангренозных процессах под действием препарата отмечается самопроизвольное отторжение некротических масс в очагах отторжения с восстановлением кожного покрова. При открытых ранах и ожогах наблюдается анальгезирующее действие.
При раздраженной и поврежденной слизистой оболочки носа, возникающей вследствие ОРВИ, ОРЗ при применении препарата могут быть ощущения зуда и жжения.
Нарушения обоняния при COVID-19: обзор медикаментозных вариантов лечения
Как восстановить обоняние у пациентов при COVID-19? Эффективность применяемых методов в мировой практике. Обзор распространенности нарушений обоняния при COVID-19. Лекарственные и не лекарственные методы во врачебной практике, восстанавливающие обоняние.
Как восстановить обоняние у пациентов при COVID-19? Эффективность применяемых методов в мировой практике. Обзор распространенности нарушений обоняния при COVID-19. Лекарственные и не лекарственные методы во врачебной практике, восстанавливающие обоняние.
При COVID-19, помимо общих симптомов (кашель, лихорадка и усталость), во всех странах сообщают об увеличении числа пациентов с потерей обоняния и вкуса. Изменения восприятия запахов отмечалось ранее и при других вирусных инфекциях (парагриппе, риновирусе, атипичной пневмонии и др.), но с намного меньшей частотой, чем у заражённых SARS-CoV-2. Патофизиология постинфекционной потери обоняния в настоящий момент рассматривается в многочисленных отечественных и зарубежных обзорах.
Вопрос о том, как восстановить обоняние, стоит довольно остро, так как во всем мире ежедневно возрастает количество людей с коронавирусной инфекцией COVID-19, а следовательно, и с данным симптомом. Дело в том, что обонятельная дисфункция влияет на качество жизни. Люди с потерей обоняния сталкиваются с проблемами при приготовлении пищи, определения ее свежести. Часто изменяется пищевое поведение – наблюдается снижение аппетита вплоть до безразличия к еде. Обонятельная дисфункция ассоциирована с множественными сопутствующими заболеваниями, включая депрессию, нарушение когнитивных функций и снижение питания. Вернуть обоняние необходимо также для предупреждения об опасностях в повседневной жизни: запахи газа, дыма, гари, кислот, щелочей и спиртов зачастую являются первым сигналом, который позволяет человеку сохранить жизнь и здоровье. 3
Терминология, применимая к изменениям обоняния:
Расстройства идентификации (дизосмия):
Распространенность нарушений обоняния при COVID-19
20 ноября 2020 г Jeyasakthy Saniasiaya и Md Asiful Islam опубликован метаанализ 27 492 пациентов «Распространенность обонятельной дисфункции при коронавирусной болезни 2019 (COVID? 19)».
В целом распространенность данного симптома у пациентов с COVID-19 составила 47,85%. Из анализа подгрупп выявлена обонятельная дисфункция у 54,40% европейских, 51,11% североамериканских, 31,39% азиатских и 10,71% австралийских пациентов с COVID-19. Кроме того, аносмия, гипосмия и дизосмия наблюдались у 35,39%, 36,15% и 2,53% пациентов с COVID-19 соответственно. Интересно, что обонятельная дисфункция была выше у нетяжелых пациентов по сравнению с тяжелыми пациентами с COVID-19 (47,48% против 9,02%).[4]
Обзор вариантов лечения с рекомендациями
В августе 2020 г Hura N, Xie DX, Choby GW опубликовали научно обоснованный обзор с рекомендациями «Лечение поствирусной обонятельной дисфункции» [5], резюмирующий данные по целесообразности применения различных средств, восстанавливающих обоняние. Оценка рекомендаций включала совокупную степень доказательности (от A до D). Цель рекомендаций заключалась в том, чтобы сопоставить качество исследования с потенциальным балансом пользы и вреда при потере обоняния.
Системные стероиды (преднизолон, метилпреднизолон, бетаметазон)
Было проведено шесть исследований с целью восстановить обоняние с применением системных стероидов. Продолжительность наблюдения, обонятельного тестирования и дозирования системных стероидов широко варьировалась. В целом 4 исследования показали умеренную пользу от системных стероидов 8, в то время как дизайн других исследований не позволял сделать окончательные выводы о возможности вернуть обоняние с помощью данной категории средств. [10,11]
Резюме:
Местные стероиды
В четырех исследованиях оценивали эффект местных кортикостероидов, включая пропионат флутиказона, спрей беклометазона и инъекции дексаметазона или бетаметазона как средств, восстанавливающих обоняние. 12
Нестероидные местные препараты
3 исследования изучали цитрат натрия для интраназального введения при потере обоняния. Кроме того, в одном идентифицированном исследовании сравнивали интраназальный инсулин с солевым раствором плацебо. 16 Но поскольку это единичное пилотное исследование, нет достаточных доказательств для включения его в обоснованное резюме.
Интраназальный цитрат натрия
Нестероидные пероральные препараты
В качестве восстанавливающих обоняние препаратов также изучались пероральные средства: антибиотики, витамин А, альфа-липоевая кислота. Для данной группы характерно невысокое качество клинических исследований. Сульфат цинка имеет 3 исследования с лучшим дизайном – вывод по нему вынесен отдельно, хотя не было обнаружено значительной эффективности в восстановлении обоняния у пациентов, получавших сульфат цинка в различных схемах. 20
Антибиотики. В двух исследованиях оценивалась способность различных антибиотиков восстановить обоняние. В первом не было различий TDI между группой, получавшей миноциклин, и группой, получавшей плацебо. Во втором не было обнаружено общего улучшения показателей идентификации запахов после лечения, однако пациенты с потерей обоняния улучшили пороги обнаружения запаха после лечения. 23
Витамин А также не продемонстрировал однозначных результатов при применении с целью вернуть обоняние. Duncan et al. в 1962 г. сообщили об улучшении субъективной обонятельной функции. В двойном слепом рандомизированном плацебо-контролируемом исследовании Reden et al. сравнивали эффективность применения 10 000 МЕ витамина А в день в течение 3 месяцев и плацебо. В то время как показатели TDI значительно увеличились у всех пациентов, не было существенной разницы между группами плацебо и принимавшими витамин А. [24,25]
Альфа-липоевая кислота, обычно используемая для лечения диабетической невропатии, была исследована Hummel et al. в качестве средства, восстанавливающего обоняние. TDI улучшился после 4,5 месяцев приема альфа-липоевой кислоты 600 мг/ день, но не достиг минимальной клинически значимой разницы.[26]
Пероральные антибиотики, витамин А, альфа-липоевая кислота.
Пероральный сульфат цинка
Обонятельная тренировка
Обонятельная тренировка относится к методам, позволяющим восстановить обоняние без дополнительной лекарственной нагрузки на организм пациента. Эффективность обонятельной тренировки оценивали всего десять исследований. 33. В большинстве работ использовался протокол, включающий воздействие четырех запахов два раза в день в течение как минимум 12 недель.
В 4 исследованиях, сравнивающих обонятельную тренировку с отсутствием лечения, было обнаружено, что обонятельная тренировка дает статистически лучшие результаты и позволяет вернуть обоняние. [27,29,32,33]. Также исследователи пришли к выводу, что долгосрочные тренировки превосходят краткосрочные со значительно более высоким средним баллом TDI через 56 недель, хотя обе группы показали наибольшее улучшение обоняния в течение первых 16 недель. [33] Интересно, что чем короче продолжительность потери обоняния до начала лечения, тем выше эффект от восстанавливающих обоняние процедур. Damm et al. продемонстрировали больший эффект от обонятельной тренировки с запахами с высокой концентрацией по сравнению с запахами с низкой концентрацией у пациентов с длительностью ВОБЛ менее 12 месяцев. [30]
Poletti et al. провели проспективное псевдорандомизированное исследование, в котором пациенты, чтобы вернуть обоняние, проводили тренировки с использованием одорантов с низкой молекулярной массой ( 150 г / моль). В этом исследовании они пришли к выводу, что одоранты с высокой молекулярной массой превосходят пороговые значения по сравнению с одорантами с низкой молекулярной массой у пациентов с потерей обоняния.
Практические вопросы обонятельной тренировки
Для применения в обонятельной тренировке наиболее простыми и эффективными являются эфирные масла. Эфирные масла имеют высокую молекулярную массу и сложный химический состав: они содержат два или три основных компонента, преимущественно это терпены, терпеноиды и фенилпропаноиды.
При выборе эфирного масла для применения с целью вернуть обоняние важно обратить внимание на качество продукта. В продаже представлено большое количество суррогатных эфирных масел, представляющих собой растительное масло с небольшим процентом эфирного масла (нарушается условие высокой концентрации запаха) или искусственным ароматизатором с низкой молекулярной массой, которые не будут обладать достаточной эффективностью и не помогут восстановить обоняние.
Также открыт вопрос комплаентности тренировок – потеря обоняния и другие нарушения восприятия запахов при COVID-19 продолжаются после окончания изоляции пациентов, а проведение тренировок с применением 4 запахов у части пациентов, ввиду занятости и образа жизни, часто вызывает сложности, несмотря на желание вернуть обоняние.
Альтернативным решением, легко реализуемым в дороге или на работе, является применение одной смеси из эфирных масел. В России представлено «Масло Дыши» (АО «Аквион»), которое на 100% состоит только из эфирных масел. Доминирующими запахами в составе композиции являются мята и эвкалипт, что позволяет концентрироваться на идентификации именно этих двух ароматов поочередно в ходе тренировок, восстанавливающих обоняние, когда невозможно провести полноценное занятие с 4 маслами.
Отличительной особенностью «Масла Дыши» является высокий стандарт качества и безопасности: средство применяется для профилактики в комплексной терапии респираторных инфекций и ринитов у детей, по нему проведено более 11 клинических исследований (подробнее: https://clck.ru/SZWdc), подтвердивших высокий профиль безопасности и эффективность. Поставщиком сырья является немецкая компания Freu&Lau с европейским уровнем контроля качества. Для повышения комплаентности есть форма в виде пластыря на одежду, браслета на руку, спрея и масла с дозатором. https://clck.ru/SUpek
Обонятельная тренировка
В целом было выявлено, что обонятельная тренировка улучшает обонятельные функции во всех 10 исследованиях. Установлено, что более эффективно восстановить обоняние помогают более высокие концентрации и молекулярная масса запахов, более длительная продолжительность обонятельных тренировок и различные запахи, используемые для них. Чем меньший временной интервал между появлением нарушений обоняния и началом тренировок, тем лучший результат показывают процедуры. В качестве альтернативы при отказе от комплексных тренировок пациентами с потерей обоняния, можно рассмотреть вариант с применением Масла Дыши. Помимо обонятельной тренировки медицинские работники после оценки рисков могут предложить курс системных или местных стероидов в качестве средств, восстанавливающих обоняние.
Лечение острых респираторных заболеваний у детей
Острые респираторные заболевания (ОРЗ) — большая группа инфекций, которые имеют много общего в патогенезе и путях передачи: речь идет в основном о воздушно-капельных инфекциях, хотя и контактный (через грязные руки) путь передачи играет не меньшую роль.
Острые респираторные заболевания (ОРЗ) — большая группа инфекций, которые имеют много общего в патогенезе и путях передачи: речь идет в основном о воздушно-капельных инфекциях, хотя и контактный (через грязные руки) путь передачи играет не меньшую роль. Этим термином принято объединять острые неспецифические инфекции вне зависимости от их локализации — от ринита до пневмонии. Однако как клинический диагноз ОРЗ требует расшифровки: должно быть указание либо на органное поражение (отит, бронхит, фарингит и т. д.), для которого известен спектр возбудителей, либо на возможную этиологию заболевания (вирусное, бактериальное ОРЗ). Поскольку до 90% ОРЗ вызваны респираторными вирусами и вирусами гриппа в отсутствие признаков бактериальной инфекции оправдан термин «острая респираторно-вирусная инфекция» (ОРВИ) и назначение противовирусной терапии.
По данным авторов серии работ, выполненных под эгидой ВОЗ, в разных странах — как развитых, так и развивающихся — дети раннего возраста ежегодно переносят 5–8 ОРЗ, причем в сельской местности они болеют реже, чем в городах, где ребенок может переносить 10–12 инфекций в год. Дети, которые в раннем детстве реже контактируют с источниками инфекции и поэтому меньше болеют в этот период, «добирают недостающие инфекции» в начальной школе. Констатация этого факта, конечно, не должна быть причиной развития фатализма в отношении ОРВИ — детей следует закалять и по возможности ограждать от источников заражения, полноценно кормить и лечить заболевания (хронический тонзиллит, аллергию), на фоне которых ОРЗ развивается особенно часто. В то же время необходимо всемерно ограждать заболевших детей от излишних терапевтических вмешательств, поскольку именно ОРЗ являются поводом для необоснованного лечения и наиболее частой причиной побочного действия лекарств.
Противовирусные средства
Строго говоря, противовирусная терапия показана при любом респираторно-вирусном заболевании. К сожалению, противовирусные средства, имеющиеся в нашем распоряжении, часто не дают выраженного эффекта, да и легкость большинства эпизодов ОРВИ, ограничивающихся 1–3 лихорадочными днями и катаральным синдромом в течение 1–2 нед, не оправдывает проведения химиотерапии. Но в более тяжелых случаях, особенно при гриппе, противовирусные средства дают определенный эффект и должны применяться шире, чем это считается целесообразным сегодня.
Основное правило применения противовирусных химиопрепаратов — их назначение в первые 24–36 ч болезни, в более поздние сроки их эффект не виден. Основным противогриппозным средством, действующим также и на ряд других вирусов [1], является римантадин, который подавляет репродукцию всех штаммов гриппа типа А. Римантадин также ингибирует репродукцию респираторно-синцитиальных (РС) и парагриппозных вирусов. Рекомендуется; 5-дневный курс из расчета 1,5 мг/кг/сут в 2 приема детям 3–7 лет; по 50 мг 2 раза детям 7–10 лет — 3 раза в сутки — старше 10 лет [2]. В раннем возрасте римантадин используют в виде альгирема (0,2% сироп): у детей 1–3 лет по 10 мл; 3–7 лет — по 15 мл: 1-й день 3 раза, 2–3-й дни — 2 раза, 4-й — 1 раз в день. Эффективность римантадина увеличивается при его приеме с препаратом но-шпа (дротаверином) перорально, в дозе 0,02–0,04 г — у детей 4–6 лет и 0,04–0,1 г — для пациентов 7–12 лет, особенно при нарушении теплоотдачи (холодные конечности, мраморность кожи) [3].
Сходным противовирусным действием обладает арбидол, ингибирующий слияние липидной оболочки вирусов гриппа с мембраной эпителиальных клеток. Он также является индуктором интерферона. Этот малотоксичный препарат можно назначить и при среднетяжелой ОРВИ с 2-летнего возраста: детям 2–6 лет по 50 мг на прием, 6–12 лет по 100 мг, старше 12 лет — по 200 мг на прием 4 раза в сутки. И римантадин, и арбидол сокращают лихорадочный период в среднем на 1 день как при гриппе А2, смешанных инфекциях, так и при не гриппозных ОРВИ [1].
Рибавирин (рибамидил, виразол) — противовирусный препарат, первоначально использовавшийся (в основном в США) как обладающий активностью в отношении РС-вируса при бронхиолитах у наиболее тяжелых больных с неблагоприятным преморбидным фоном (недоношенные, с бронхолегочной дисплазией). Препарат применяется для этой цели в виде постоянных (до 18 ч в сутки) ингаляций через специальный ингалятор в дозе 20 мг/кг/сут; из-за высокой цены и побочных явлений в Европе практически не применяется. Оказалось также, что этот препарат активен в отношении вирусов гриппа, парагриппа, простого герпеса, аденовирусов, а также коронавируса — возбудителя тяжелого острого респираторного синдрома (ТОРС — SARS). При гриппе у подростков старше 12 лет его применяют внутрь в дозе 10 мг/кг/сут в течение 5–7 дней. При ТОРС рибавирин вводят внутривенно.
Прогресс в отношении лечения гриппа, вызываемого вирусами как типа А, так и типа В, может быть связан с использованием ингибиторов нейраминидазы озельтамивир — тамифлю и занамивир — реленца. Эти препараты при раннем приеме уменьшают длительность лихорадки на 24–36 ч и обладают профилактическим действием, но опыта их применения у детей (с 12 лет) в России мало, да и в справочниках последних лет о них практически не пишут. Реленца применяется в виде ингаляций порошка (в США с 7 лет) — по 2 ингаляции (5 мг каждая) в день с интервалом не менее 2 ч (в 1-й день) и 12 ч (со 2-го по 5-й день лечения). Тамифлю (капсулы по 75 мг и суспензия 12 мг/мл) у взрослых и детей с 12 лет используется по 75 мг 1 раз в день в течение 5 дней (в США дозы для детей 1–12 лет: весом до 15 кг — 30 мг 2 раза в день, 15–23 кг — 45 мг 2 раза в день, 23–40 кг — 60 мг 2 раза в день). Этот препарат — единственный, к которому чувствителен птичий грипп H5N1, и в настоящее время ряд стран производят его накопление на случай эпидемии, что, видимо, ограничивает его применение при относительно небольшом производстве (Хоффман-Ля Рош, Швейцария, выпускает 7 млн доз тамифлю в год).
Используемые местно (в нос, в глаза) препараты флореналь 0,5%, оксолиновая мазь 1–2%, бонафтон, локферон и другие обладают некоторой противовирусной активностью; они показаны, например, при аденовирусной инфекции. Хотя их эффект оценить трудно, низкая токсичность оправдывает применение этих средств.
Протеолитические процессы, происходящие при синтезе вирусных полипептидов, а также слияние вирусов с мембранами клеток способны ингибировать апротинины — контрикал, гордокс и др., а также амбен. Эти препараты могут использоваться при тяжелых формах респираторных инфекций с высокой активностью воспаления, обычно при признаках ДВС-синдрома (как ингибиторы фибринолиза) и расстройствах микроциркуляции. Амбен входит в состав гемостатических губок. Контрикал используют в дозе 500–1000 ЕД/кг/сут. Применяемые у взрослых олифен и эрисод, входящие в состав препаратов этой группы, у детей пока не апробированы.
Интерфероны и их индукторы обладают универсальными противовирусными свойствами, подавляя репликацию как РНК, так и ДНК, стимулируя одновременно иммунологические реакции макроорганизма. Раннее применение интерферонов способно если и не оборвать течение инфекции, то смягчить ее проявления.
Лаферон — порошок интерферона α-2β — используют в виде капель в нос, а у детей старше 12 лет его вводят внутримышечно по 1–3 млн МЕ.
Помимо арбидола, в качестве индукторов интерферона используют ряд препаратов. Наибольшую популярность у детей старше 7 лет завоевал амиксин (тилорон) — его вводят при первых симптомах ОРЗ или гриппа внутрь после еды по 60 мг 1 раз в день на 1-й, 2-й, и 4-й день от начала лечения. Детский анаферон — гомеопатические дозы афинно очищенных антител к интерферону α, его применяют по 1 таблетке каждые 30 мин в течение 2 ч, далее 3 раза в сутки, однако убедительных данных о его эффективности пока собрано мало.
У детей, больных ОРВИ, часто приходится лечить первичную герпесвирусную инфекцию, протекающую как тяжелый фебрильный стоматит. У детей с атопическим дерматитом часто развивается экзема Капоши — герпесвирусная инфекция пораженной кожи, также протекающая тяжело. У старших детей ОРВИ — самая частая причина реактивации герпес-вирусов в виде специфических высыпаний на губах, крыльях носа, реже — на гениталиях. Эта инфекция хорошо поддается лечению ацикловиром — его применяют по 20 мг/кг/сут в 4 приема, в тяжелых случаях — до 80 мг/кг/сут или внутривенно по 30–60 мг/кг/сут. Валацикловир не требует дробного введения, его доза для взрослых и подростков старше 12 лет составляет 500 мг 2 раза в день.
Для лечения ОРВИ на практике применяется значительно большее число средств, в том числе растительного происхождения (адаптогены, БАД, настойки и т. д.). В отношении эффективности подавляющего большинства из них данных не существует, однако с побочными их воздействиями сталкиваться приходится часто.
Антибактериальные средства
Бактериальные ОРЗ у детей, как и у взрослых, относительно немногочисленны, но именно они представляют наибольшую угрозу в плане развития серьезных осложнений. Постановка диагноза бактериального ОРЗ у постели остро заболевшего ребенка представляет большие трудности ввиду сходства многих их проявлений с таковыми при ОРВИ (повышение температуры, насморк, кашель, боли в горле), а экспресс-методы этиологической диагностики практически недоступны. Да и выявление микробного возбудителя в материале дыхательных путей еще не говорит о его этиологической роли, поскольку большинство бактериальных заболеваний вызываются возбудителями, постоянно вегетирующими в дыхательных путях.
В этих условиях, естественно, врач при первом контакте с ребенком склонен переоценивать возможную роль бактериальной флоры и использовать антибиотики чаще, чем это необходимо. Наши данные показывают, что в Москве антибиотики назначают 25% детей с ОРВИ, в некоторых городах России эта цифра достигает 50–60%. Та же тенденция характерна и для других стран: антибиотики при ОРВИ используют у детей в 14–80% случаев [6, 7]. Близкие к нашим данным показатели приводят авторы из Франции (24% [8]) и США (25% [9]). В развивающихся странах антибактериальные препараты при ОРЗ применяются также излишне широко, хотя этот процесс сдерживается более низкой их доступностью. В Китае антибиотики получают 97% детей с ОРЗ, обратившихся за медицинской помощью [10]. Очевидно, что при вирусной этиологии заболевания антибиотики по меньшей мере бесполезны и, скорее всего, даже вредны, поскольку они нарушают биоценоз дыхательных путей и тем самым способствуют заселению их несвойственной, чаще кишечной, флорой [11].
Антибиотики у детей с ОРВИ чаще, чем при бактериальных заболеваниях, вызывают побочные действия — различные сыпи и другие аллергические проявления. При бактериальных процессах в организме происходит мощный выброс ряда медиаторов (например, циклического аденозина монофосфата), препятствующих манифестации аллергических проявлений. При вирусных инфекциях этого не происходит, поэтому аллергические реакции реализуются намного чаще.
Другая опасность избыточного применения антибиотиков — распространение лекарственно-устойчивых штаммов пневмотропных бактерий, отмечающееся во многих странах мира. Очевидно, что неоправданное применение антибиотиков ведет и к излишним расходам на лечение.
Не следует игнорировать и влияние антибиотиков на становление иммунной системы ребенка. Характерное для новорожденного преобладание иммунного Т-хелперного ответа 2-го типа (Тh-2) уступает более зрелому Т-хелперному ответу 1-го типа (Тh-1) в значительной степени под влиянием стимуляции эндотоксинами и другими продуктами бактериального происхождения. Такая стимуляция происходит как во время бактериальной инфекции, так и во время ОРВИ, поскольку и вирусная инфекция сопровождается усиленным (хотя и неинвазивным) размножением пневмотропной флоры [11]. Естественно, применение антибиотиков ослабляет или вообще подавляет эту стимуляцию, что, в свою очередь, способствует сохранению Тh-2-направленности иммунного ответа, повышающей риск аллергических проявлений и снижающей интенсивность противоинфекционной защиты.
Показания к антибактериальному лечению ОРЗ
В рекомендациях профессиональных обществ педиатров большинства стран подчеркивается важность отказа от применения антибактериальных средств у детей с неосложненной респираторно-вирусной инфекцией. В рекомендациях Академии педиатрии США подчеркивается, что антибиотики не используют не только при неосложненной ОРВИ, но и слизисто-гнойный насморк также не является показанием к назначению антибиотиков, если он длится менее 10–14 дней [8]. Французский консенсус допускает применение антибиотиков при ОРВИ лишь у детей с рецидивами отита в анамнезе, у малышей в возрасте до 6 мес, если они посещают ясли и при наличии иммунодефицита [9].
В рекомендациях Союза педиатров России указано, что при неосложненных ОРВИ системные антибиотики в подавляющем большинстве случаев не показаны [4]. В этом документе перечисляются наблюдающиеся в первые 10–14 дней проявления болезни, которые не могут оправдать введения антибиотиков.
Вопрос о назначении антибиотиков у ребенка с ОРВИ возникает, если у него в анамнезе есть рецидивирующий отит, неблагоприятный преморбидный фон (выраженная гипотрофия, врожденные пороки развития) или при наличии клинических признаков иммунодефицита.
Ниже приведены признаки бактериальной инфекции, требующие антибактериального лечения:
Чаще, чем эти явные очаги, педиатр видит лишь косвенные симптомы вероятной бактериальной инфекции, среди которых наиболее часто выявляются стойкая (3 дня и более) фебрильная температура, одышка в отсутствие обструкции (частота дыхания выше 60 в 1 мин у детей 0–2 мес жизни, более 50 в 1 мин в возрасте 3–12 мес и более 40 — у детей 1–3 лет), асимметрия аускультативных данных в легких. Такая симптоматика заставляет назначить антибиотик, который, в случае если диагноз при последующем обследовании не подтвердился, следует тут же отменить.
Для стартовой терапии бактериальных ОРЗ используют небольшой набор антибиотиков. При отите и синусите для подавления основных возбудителей — пневмококка и гемофильной палочки назначают амоксициллин внутрь 45–90 мг/кг/сут. У недавно получавших антибиотики детей используют амоксициллин/клавуланат 45 мг/кг/сут, подавляющий рост вероятно устойчивых у этих больных гемофильной палочки и моракселлы.
Острый тонзиллит требует дифференциальной диагностики между аденовирусной ангиной, инфекционным мононуклеозом и стрептококковым тонзиллитом. Для вирусной ангины характерен кашель, катаральный синдром, для стрептококковой — отсутствие кашля, для мононуклеоза — изменения крови. Антибиотики (пенициллин фау, цефалексин, цефадроксил) показаны при стрептококковом тонзиллите; применение амоксициллина нежелательно, поскольку при мононуклеозе он способен вызывать токсические сыпи. Хотя аденовирусная ангина не требует назначения антибиотика, наличие выраженного лейкоцитоза (15–25х10 9 /л) и повышение уровня С-реактивного белка оправдывают их применение во многих случаях.
Бронхит, как правило, представляет собой вирусное заболевание, не требующее антибактериального лечения. Исключение составляют бронхиты, вызванные микоплазмой, при их выявлении показано использование макролидов (азитромицин, мидекамицин и др.). Клиническими признаками микоплазменного бронхита являются:
Выбор антибактериальных средств для стартового лечения внебольничной пневмонии также не очень велик, поскольку бoльшая часть «типичных» пневмоний вызывается пневмококком или гемофильной палочкой (исключение — первые месяцы жизни, когда возбудителем могут быть стафилококки и кишечная флора), тогда как «атипичные» формы поддаются лечению макролидами. Выбор стартового антибиотика при пневмонии определяется с учетом вероятного возбудителя заболевания.
При типичной пневмонии (фебрильная, с очагом или гомогенным инфильтратом) применяют:
При атипичной (с негомогенным инфильтратом) пневмонии:
Патогенетические методы лечения
К этим методам можно отнести вмешательства, применяемые при остром ларингите и обструктивных формах бронхита.
Острый ларингит, круп представляют собой состояния, требующие оценки степени стеноза, о чем судят по интенсивности инспираторных втяжений грудной клетки, частоте пульса и дыхания. Круп 3-й степени требует неотложной интубации, круп 1-й и 2-й степени лечится консервативно. Больному с ларингитом антибиотики не вводят, согласно всемирному консенсусу наиболее эффективно введение дексаметазона внутримышечно 0,6 мг/кг, что останавливает прогрессирование стеноза. Дальнейшее лечение продолжают ингаляционными стероидами (дозированными или через небулайзер — пульмикорт) в комплексе со спазмолитиками (сальбутамол, беротек, беродуал в ингаляциях).
Стеноз гортани может быть вызван эпиглоттитом (в его этиологии основная роль принадлежит H. influenzae типа b) — для него характерны высокая температура и усиление стеноза в положении на спине; назначение антибиотика (цефуроксим, цефтриаксон) в данном случае обязательно.
Затруднение дыхания и экспираторная одышка часто наблюдаются при бронхиолите и обструктивном бронхите, а также при приступе астмы на фоне ОРВИ. Поскольку бактериальная инфекция в таких случаях — редкость, назначение антибиотиков не оправдано. Лечение — ингаляции симпатомиметиков (у маленьких детей лучше в комбинации с ипратропия бромидом) и применение стероидов в рефрактерных случаях — дает возможность справиться с обструкцией за 1–3 дня.
Симптоматическая терапия ОРЗ
Как указано выше, ОРЗ — наиболее часто встречающаяся причина применения лекарств, в частности симптоматических средств, которые занимают бoльшую часть аптечных полок. Важно, однако, четко представлять себе, что одно лишь наличие того или иного симптома не должно быть основанием для вмешательства, надо прежде всего оценить, в какой степени этот симптом нарушает жизнедеятельность и не окажется ли лечение опаснее симптома.
Лихорадка сопровождает большинство ОРЗ и является защитной реакцией, так что снижение ее уровня жаропонижающими средствами оправдано лишь в определенных ситуациях. К сожалению, многие родители да и врачи считают лихорадку наиболее опасным проявлением болезни и стремятся нормализовать температуру во что бы то ни стало. Согласно проведенным нами исследованиям [12], жаропонижающие получают 95% детей с ОРВИ, в том числе 92% детей с субфебрильной температурой. Такую тактику нельзя считать рациональной, поскольку лихорадка как компонент воспалительного ответа организма на инфекцию во многом носит защитный характер.
Жаропонижающие не влияют на причину лихорадки и не сокращают ее длительность, они увеличивают период выделения вирусов при ОРЗ [12, 13]. При большинстве инфекций максимум температуры редко превышает 39,5°. Такая температура не таит в себе какой-либо угрозы для ребенка старше 2–3 месяцев; обычно, чтобы наступило улучшение самочувствия, бывает достаточно понизить ее на 1–1,5°. Показания для снижения температуры [4]:
Наиболее безопасным жаропонижающим для детей является парацетамол, его разовая доза составляет 15 мг/кг, суточная — 60 мг/кг. Ибупрофен (5–10 мг/кг на прием) чаще дает побочные эффекты (при сходном жаропонижающем эффекте), его рекомендуют использовать в случаях, когда требуется противовоспалительный эффект (артралгии, мышечные боли и т. д.).
При ОРЗ у детей не применяются ацетилсалициловая кислота (аспирин) — в связи с развитием синдрома Рея, метамизол натрия (анальгин) внутрь (опасность агранулоцитоза и коллаптоидного состояния), амидопирин, антипирин, фенацетин. Нимесулид гепатотоксичен; к сожалению, его детские формы были зарегистрированы в России, хотя они не применяются больше нигде в мире.
Лечение насморка сосудосуживающими каплями улучшает носовое дыхание лишь в первые 1–2 дня болезни, при более длительном применении они могут усиливать насморк, а также вызывать побочные явления. В раннем возрасте из-за болезненности используют только 0,01% и 0,025% растворы. Удобны (после 6 лет) назальные спреи, позволяющие при меньшей дозе равномерно распределить препарат (длянос, виброцил). Но наиболее эффективно очищает нос и носоглотку, особенно при густом экссудате, физиологический раствор (или его аналоги, в том числе приготовленный дома раствор поваренной соли: на 1/2 стакана воды добавить соли на кончике ножа) — по 2–3 пипетки в каждую ноздрю 3–4 раза в день в положении лежа на спине со свешивающейся вниз и назад головой. Орально применяющиеся средства от насморка, содержащие симпатомиметики (фенилэфрин, фенилпропаноламин, псевдоэфедрин) используют после 12 лет, с 6 лет назначают фервекс для детей, не содержащий этих компонентов. Противогистаминные препараты, в том числе второго поколения, эффективные при аллергическом рините, ВОЗ не рекомендует применять при ОРЗ [15].
Показанием для назначения противокашлевых средств (ненаркотические центрального действия — глауцин, бутамират, окселадин) является только сухой кашель, который при бронхитах обычно быстро становится влажным. Отхаркивающие средства (их действие, стимулирующее кашель, аналогично рвотному) имеют сомнительную эффективность и у маленьких детей могут вызывать рвоту, а также аллергические реакции — вплоть до анафилаксии. Их назначение скорее дань традиции, чем необходимость, дорогие средства из этой группы не имеют преимуществ перед обычными галеновыми, ВОЗ вообще рекомендует ограничиться «домашними средствами» [15].
Из числа муколитиков наиболее активен ацетилцистеин, но при острых бронхитах у детей нужды в его применении практически нет; карбоцистеин назначают при бронхите — в расчете на его благоприятное влияние на мукоцилиарный клиренс. Амброксол при густой мокроте применяют как внутрь, так и в ингаляциях. Аэрозольные ингаляции муколитиков используют при хронических бронхитах; аэрозольные ингаляции воды, физраствора и прочее при ОРЗ не показаны.
При длительно сохраняющемся кашле (коклюш, упорный трахеит) показаны противовоспалительные средства: ингаляционные стероиды, фенспирид (эреспал). Смягчающие пастилки и спреи при фарингите обычно содержат антисептики, их применяют с 6 лет; начиная с 30 мес используют антибиотик местного действия фюзафюнжин, выпускаемый в аэрозоле (биопарокс) и применяемый как назально, так и орально.
Все еще популярные в России при бронхитах горчичники, банки, жгучие пластыри у детей применяться не должны; при ОРЗ редко возникают показания для физиотерапии. Удивление вызывает популярность галокамер, пребывание в которых имеет целью «ингаляцию паров поваренной соли», как в соляной шахте. Но в соляной шахте на пациента воздействует не соль (которая к летучим субстанциям никак не относится), а чистый воздух, свободный от пыли и других аллергенов; кроме того, находятся там не по 15 мин. Лечение в галокамере не значится и в консенсусе по астме, тем не менее многие поликлиники тратят огромные деньги на их сооружение.
Указанные в этом разделе средства, за немногими исключениями, нельзя считать обязательными при ОРВИ; более того, мы сплошь и рядом сталкиваемся с побочными явлениями, возникшими в результате такого лечения. Поэтому следует взять за правило минимизацию лекарственных нагрузок в случаях нетяжелых ОРВИ.
Проблема ОРЗ в детском возрасте остается актуальной не только из-за их распространенности, но и в связи с необходимостью пересмотра и оптимизации лечебной тактики. Накопленные данные показывают, что преобладающие в практике педиатров подходы по меньшей мере не способствуют становлению иммунной системы ребенка, поэтому пересмотр тактики должен быть в первую очередь направлен на модификацию терапевтической активности, в частности на снижение случаев неоправданных назначений антибактериальных и жаропонижающих средств.
Литература
В. К. Таточенко, доктор медицинских наук, профессор
НЦЗД РАМН, Москва