полинадим можно капать в нос
Полинадим
Препарат полинадим представляет собой капли для глаз, в состав которых входит нафтизин и димедрол, обладающие противовоспалительным и антиаллергическим действием. Этот препарат в короткие сроки суживает сосуды конъюнктивы, в связи с чем уменьшает отек при аллергических реакциях, воспалении и инфекции.
Состав и форма выпуска
В 1 мл раствора Полинадим содержится два активных компонента:
Среди вспомогательных компонентов выделяют:
Выпускается препарат в виде раствора для закапывания в глаза во флаконах-капельницах из темного стекла или полиэтилена. Флакон вместе с инструкцией помещен в картонную упаковку.
Фармакологическое действие
Действие капель Полинадим связано с эффектами каждого из компонентов. Димедрол является противоаллергическим препаратом, который блокирует гистаминовые рецепторы (Н1), тем самым уменьшая выраженность слезотечения, отека и зуда.
Нафтизин относится к сосудосуживающим лекарствам, за счет чего при местном применения уменьшает выраженность отека и воспаления.
Показания
Капли для глаз Полинадим используют при острых аллергических и поллинозных конъюнктивитах.
Эффективен препарат и в отношении конъюнктивита аллергической природы, связанного с использованием лекарственных средств.
Назначают эти глазные капли и в качестве дополнительной меры при лечении инфекционных заболеваний глазного яблока, которые сопровождаются аллергическим компонентом.
Способ применения
В период обострений у взрослых пациентов выполняют закапывание одной капли Полинадима в конъюнктивальный мешок каждые три часа до тех пор, пока не уменьшатся явления отека и раздражения. После этого кратность приема сокращают до 2-3 в сутки до тех пор, пока имеются клинические проявления.
Детям старше двух лет производят закапывание препарата по 1-2 капли в сутки.
Если применяют Полинадим более пяти дней, следует предварительно согласовать лечебную тактику с врачом.
Если на фоне терапии препаратом Полинадим в течение трех суток сохраняются симптомы раздражения конъюнктивы, то следует отменить лекарство и обратиться к офтальмологу очно.
Противопоказания
Противопоказано применение Полинадима при:
Не применяют лекарство у детей в возрасте младше двух лет, у беременных женщин и в период лактации.
Осторожности требует назначение Полинадима у пациентов с:
Побочные действия
При применении препарата Полинадим нередко возникают местные побочные эффекты:
Местные реакции проходят вскоре после отмены препарата.
Установлен единичный случай снижения прозрачности роговицы. При этом капли применяли не менее 10 раз в сутки на протяжении семи дней. Этот эффект также исчез после отмены лекарства.
Крайне редко, обычно у пациентов детского или престарелого возраста, могут развиваться системные явления:
Передозировка
Если использовать препарат Полинадим согласно инструкции, то возникновение передозировки маловероятно.
При продолжительном и частом приеме у детей дошкольного возраста это лекарство может приводить к угнетению функции центральной нервной системы, продолжительному расширению зрачка, учащенному пульсу и гипертензии, снижению системной температуры тела. При этом показано проведение симптоматической терапии.
Взаимодействия
На фоне приема Полинадима вместе с трициклическими антидепрессантами существует угроза усиления эффектов нафтизина.
При совместном назначении с препаратами, относящимися к ингибиторам МАО, возможно развитие гипертонического криза. При этом риск сохраняется на протяжении десяти дней после отмены лекарства.
Особые указания
Не стоит закапывать лекарство чаще, чем каждые три часа и дольше, чем пять дней.
Нельзя использовать раствор для приема внутрь или введения парентерально.
Не рекомендуется носить в период терапии мягкие контактные линзы. В случае если отказ от линз невозможен, их удаляют перед закапываниями и помещают на поверхность роговицы лишь спустя 15 минут после этого.
Так как препарат может временно ухудшить зрение, не рекомендуется непосредственно после инстилляции управлять автомобилем или работать с механизмами.
После вскрытия флакона раствор годен не более месяца. В закрытом состоянии его можно хранить на протяжении двух лет.
Цена препарата Полинадим
Стоимость препарата «Полинадим» в аптеках Москвы начинается от 30 руб.
Аналоги Полинадима
Нафтизин
Визин
Октилия
Аллергодил
Обратившись в «Московскую Глазную Клинику», Вы сможете пройти обследование на самом современном диагностическом оборудовании, а по его результатам – получить индивидуальные рекомендации ведущих специалистов по лечению выявленных патологий.
Клиника работает семь дней в неделю без выходных, с 9 до 21 ч. Записаться на прием и задать специалистам все интересующие Вас вопросы можно по телефонам 8 (800) 777-38-81 и 8 (499) 322-36-36 или онлайн, воспользовавшись соответствующей формой на сайте.
Заполните форму и получите скидку 15 % на диагностику!
Опыт применения комбинированных препаратов при лечении ринитов и синуситов у детей
Заболеваемость синуситами до настоящего времени достаточно высока. По данным различных авторов, заболеваниями носа и околоносовых пазух страдает от 17 до 22% детского населения. Одним из существенных факторов патогенеза острых
Заболеваемость синуситами до настоящего времени достаточно высока. По данным различных авторов, заболеваниями носа и околоносовых пазух страдает от 17 до 22% детского населения. Одним из существенных факторов патогенеза острых и особенно хронических воспалительных заболеваний носа и околоносовых пазух является нарушение механизма мукоцилиарного транспорта. Это чаще всего связано с отеком слизистой оболочки, избыточным образованием и повышением вязкости носового секрета, что влечет за собой расстройство дренажной, дыхательной, секреторной и обонятельной функций. Наиболее распространенный метод лечения синуситов — пероральное или внутримышечное назначение антибиотиков. Так как поступление антибиотика из кровяного русла в очаг воспаления ограничено, лечение синуситов должно носить комплексный характер.
В первую очередь это должно касаться улучшения вентиляции, а также дренажа околоносовых пазух и носоглотки.
До настоящего времени врачи-оториноларингологи не всегда практикуют назначение включенных в схему терапии больных синуситами адекватных мукорегулирующих препаратов, которые, разжижая густой вязкий секрет и улучшая мукоцилиарный клиренс, способствуют удалению секрета из пазух. Среди препаратов, воздействующих на мукоцилиарную активность, ранее использовались средства, стимулирующие разжижение ринобронхиального секрета, или так называемые муколитики, которые изменяют вязкость секрета, воздействуя на его физико-химические свойства. Речь идет о ферментах (трипсине, химотрипсине и т. д.), которые из-за наличия побочных эффектов в настоящее время не применяются.
Муколитическим действием обладают также препараты, снижающие поверхностное натяжение, т. е. воздействующие на гель-фазу отделяемого и разжижающие как мокроту, так и носоглоточный секрет. К этой группе относится флуимуцил (N-ацетилцистеин), действие которого связано со способностью свободной сульфгидрильной группы N-ацетилцистеина расщеплять межмолекулярные дисульфидные связи агрегатов гликопротеинов слизи, оказывая сильное разжижающее действие и уменьшая вязкость в отношении любого вида секрета: гнойного, слизисто-гнойного, слизистого. Особенность флуимуцила состоит в том, что помимо прямого муколитического действия N-ацетилцистеин обладает мощными антиоксидантными свойствами и способен обеспечить защиту органов дыхания от цитотоксического воздействия метаболитов воспаления, факторов окружающей среды, табачного дыма.
В группе муколитиков большой интерес представляют комбинированные препараты, а именно ринофлуимуцил, в состав которого кроме N-ацетилцистеина, разжижающего секрет, входит симпатомиметик — туаминогептана сульфат, обладающий мягким сосудосуживающим действием и не вызывающий излишней сухости слизистой оболочки. После разрыва дисульфидных мостиков слизь и мокрота теряют вязкость, начинают впитывать в себя воду и мягко удаляются при сморкании, чихании, кашле. Показаниями к применению ринофлуимуцила являются:
Оценка эффективности препарата производилась в группе из 55 пациентов в возрасте от 6 до 14 лет; ринофлуимуцил впрыскивали по одной дозе в каждую половину носа 3-4 раза в день, курс составил 6-7 дней. Состояние детей оценивали по их субъективным ощущениям до и после применения препарата, а также объективным критериям (уменьшение гиперемии и застойных явлений в слизистой оболочке, улучшение носового дыхания, уменьшение слизи, изменение ее реологических свойств).
Уже после 6-8 ингаляций ринофлуимуцила была отмечена положительная динамика.
Результат применения препарата оценивался следующим образом: 70% больных — отлично; 20% — хорошо; 10% — удовлетворительно.
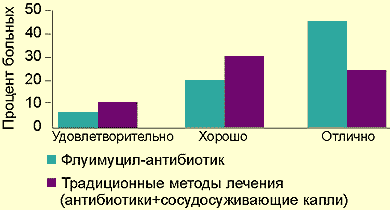 |
| Рисунок. Сравнительные результаты лечения флуимуцилом-антибиотиком ИТ и традиционными методами |
Побочных явлений от применения препарата не отмечено. Достоинство ринофлуимуцила в том, что он воздействует на поверхность слизистой оболочки и, разжижая слизь, уменьшает ее вязкость и способствует продуктивному физиологическому акту очищения полости носа.
Следующий препарат, на который следует обратить внимание, — это флуимуцил-антибиотик ИТ, соединяющий в одной лекарственной форме два компонента: N-ацетилцистеин и тиамфеникола глицинат (тиамфеникол — препарат из группы хлорамфениколов). Спектр антимикробной активности препарата представлен в табл. 1 (Клиническая фармакология антибактериальных препаратов/Под ред. Ю. Б. Белоусова, 1988).
Препарат обладает сочетанным антибактериальным и муколитическим действием и рекомендуется для лечения заболеваний органов дыхания, вызванных бактериальной инфекцией и сопровождающихся образованием густого вязкого секрета. Антимикробная активность тиамфеникола обусловлена его вмешательством в синтез бактериальных белков. Последние исследования показали, что сочетание тиамфеникола и N-ацетилцистеина позволяет препарату сохранять неконъюгированную форму и достигать очага воспаления в концентрациях, достаточных для создания бактерицидного эффекта. Препарат проявляет муколитическую активность в отношении любого вида секрета — слизистого, слизисто-гнойного, гнойного. Флуимуцил-антибиотик ИТ облегчает отделение мокроты и носовой слизи. Препарат эффективен при введении в околоносовые пазухи.
Мы располагаем данными лечения препаратом флуимуцил-антибиотик ИТ у 37 детей, из них у 17 был диагностирован острый гайморит, у 10 — обострение хронического гайморита и у 10 — обострение хронического гнойного гаймороэтмоидита. Контрольная группа пациентов лечилась традиционным методом без применения флуимуцила-антибиотика. Сравнительные данные представлены на рисунке.
Препарат использовался для промывания околоносовых пазух после пункций или после оперативного вмешательства, в том числе после эндоназального вскрытия клеток решетчатого лабиринта. Хорошие результаты были получены уже после 2-3 промываний: улучшилось носовое дыхание, сократился отек слизистой оболочки полости носа, уменьшилось количество секрета, исчез его гнойный характер. Показания и способы применения препарата представлены в табл. 2.
Эффективность флуимуцила-антибиотика ИТ определяется не только антибактериальным воздействием, но и способностью обеспечивать быстрое и полное удаление экссудата, что в свою очередь усиливает антибактериальный эффект.
Литература
Обратите внимание!
Флуимуцил-антибиотик ИТ обладает следующими фармакологическими и терапевтическими свойствами:
Лечение аллергических конъюнктивитов
Исследования последних лет указывают на гиподиагностику аллергических заболеваний глаз и недостаточно эффективно проводимую терапию их у детей и взрослых. Эти факты связаны, прежде всего, с отсутствием точных взглядов ученых на этиологические и патофиз
Исследования последних лет указывают на гиподиагностику аллергических заболеваний глаз и недостаточно эффективно проводимую терапию их у детей и взрослых. Эти факты связаны, прежде всего, с отсутствием точных взглядов ученых на этиологические и патофизиологические механизмы развития этой патологии. Сегодня для клинической практики крайне важно выработать единые подходы не только к классификации, но и к диагностике и терапии аллергических заболеваний глаз. Для этой цели следует разработать и принять международный согласительный документ, который регламентировал бы также критерии оценки степеней тяжести различных форм аллергических заболеваний глаз. Необходимо проведение объективных клинических исследований, направленных на улучшение качества лечения таких пациентов.
Между тем по эпидемиологическим данным около 15–20% населения западных стран страдает аллергическими заболеваниями глаз. Анализ недавно проведенного в США исследования NHANES III (Third National Health and Nutrition Examination Survey) показал, что такие симптомы, как «эпизоды слезотечения, зуда глаз в течение последних 12 месяцев» беспокоят 40% взрослой популяции, причем показатели распространенности подобных симптомов с возрастом достоверно не менялись [1]. Следует отметить, что одним из факторов, располагающих к возникновению у 1/5 больных глазных, назальных или риноконъюнктивальных симптомов, по данным опроса являлся контакт с кошкой; другими провоцирующими факторами выступали домашняя пыль и пыльца.
При сравнении распространенности аллергических заболеваний в двух близко расположенных друг от друга городах России (Светогорск) и Финляндии (Иматра) было установлено, что среди детей в возрасте 7–16 лет аллергическим конъюнктивитом страдают 3,2% и 4,7% школьников соответственно, причем у российских детей выраженность клинических проявлений аллергии протекала тяжелее [2].
Диагностика и клиника аллергических заболеваний глаз
Термин «аллергический конъюнктивит» включает следующие формы заболеваний: сезонный аллергический конъюнктивит, круглогодичный аллергический конъюнктивит, весенний кератоконъюнктивит, конъюнктивит с гиперплазией сосочков и атопический кератоконъюнктивит. Следует сказать, что такие клинические признаки, как гиперемия, зуд глаз и слезотечение, являются общими для всех вышеперечисленных форм аллергических конъюнктивитов. Патофизиологические механизмы развития сезонного и круглогодичного аллергических конъюнктивитов обусловлены аллергическими реакциями немедленного и замедленного типов. При хронических формах заболеваний, таких как весенний конъюнктивит у детей и атопический кератоконъюнктивит у взрослых, морфологически выявляют наличие тучных клеток, активацию эозинофилов и лимфоцитов; по мере прогрессирования заболеваний происходит разрастание соединительной ткани, приводящее к гипертрофии сосочков конъюнктивы и фиброзу. Течение атопического кератоконъюнктивита может сопровождаться осложнениями в виде язв роговицы (бактериальной, герпетической этиологий), отслойки сетчатки, кератоконуса, катаракты, стафилококкового блефарита [3]. Круглогодичный аллергический конъюнктивит также имеет хроническое течение, довольно часто в сочетании с назальными симптомами.
Для правильной диагностики аллергических конъюнктивитов необходимо проведение совместных консультаций окулиста и аллерголога-иммунолога с последующим аллергологическим обследованием пациента (кожные пробы и/или in vitro тесты). Особую трудность представляют больные с весенним кератоконъюнктивитом, из-за отсутствия точных критериев диагностики этого заболевания с неясным до сих пор патогенезом [5] (табл. 1).
Конъюнктивит с гиперплазией сосочков часто наблюдается при постоянном ношении контактных линз. Заболевание обостряется в период цветения растений весной. Основные жалобы больных — зуд в глазах и прозрачное или белое отделяемое, которое со временем становится густым. Возможные причины конъюнктивита с гиперплазией сосочков — полимерный материал контактных линз, антисептики, например, тиомерсал, отложения белка на поверхности линзы [3, 5].
Для оценки глазных симптомов разработана шкала Total Ocular Symptom Score (TOSS), включающая такие критерии, как гиперемия, зуд и слезотечение. Известно, что степень выраженности этих симптомов, изолированно или в сочетании с назальными, может сильно различаться среди больных аллергией. Возможно, это связано с недооценкой такой связи в эпидемиологических исследованиях, более мощными механизмами очищения конъюнктивальной оболочки или же меньшим контактом глаз с аллергеном [3]. Обнаружена статистически достоверная связь между аллергическим конъюнктивитом/аллергическим ринитом и развитием острого среднего отита у детей школьного возраста [6].
В исследовании, недавно проведенном в Бразилии, после уточнения диагноза 207 больных в возрасте 1–45 лет были распределены следующим образом: у 38,65% выставлен диагноз весеннего кератоконъюнктивита; 38,65% — атопический кератоконъюнктивит; 12,56% — круглогодичный аллергический конъюнктивит и в 10,14% случаев точный диагноз не был установлен [7].
Лечение
Больным, страдающим аллергическим конъюнктивитом, рекомендуют исключить контакт с аллергеном, назначают холодные компрессы, искусственные слезы, 2–4 раза в сутки. При неэффективности такого нефармакологического подхода, для улучшения контроля над глазными симптомами показана фармакотерапия следующими группами препаратов (табл. 2) [3, 5]. Например, Н1-топические антигистаминные препараты (азеластин — Аллергодил; левокабастин — глазные капли для детей в возрасте ≤ 12 лет; за рубежом широко используют селективный антагонист Н1-рецепторов олопатадин — Опатанол, начиная с возраста старше 3 лет жизни) позволяют быстро купировать глазное воспаление, однако из-за короткого периода действия их следует применять до 4 раз в сутки. При длительном использовании возможно раздражающее действие на глаз. Больным с атопией в период цветения растений следует прекратить ношение линз из-за резкого усиления симптомов аллергии в это время.
Сосудосуживающие глазные капли (тетризолин — Октилия, Визин; нафазолин) назначают на очень короткий срок, поскольку при длительном использовании они вызывают ряд серьезных побочных эффектов (жжение, мидриаз, гиперемия или медикаментозный конъюнктивит).
Для уменьшения зуда более эффективно лечение комбинированными (сосудосуживающее средство для местного применения + топический Н1-блокатор) препаратами. Например, нафазолин нитрат + антазолин мезилат (Санорин-Аналергин), антазолина гидрохлорид + тетризолина гидрохлорид (Сперсаллерг), которые используют до 4 раз в сутки.
Стабилизаторы мембраны тучных клеток (кромоглициевая кислота 2% или 4% — Лекролин, Хай-Кром, КромоГЕКСАЛ) назначают еще за 3–4 недели до предполагаемого контакта с аллергеном. Необходимость их приема не менее 4 раз в сутки резко снижает комплайнс больных. В отличие от классических мембраностабилизаторов, топические селективные Н1-блокаторы оказывают двойной эффект: ингибируют дегрануляцию тучных клеток и блокируют H1-рецепторы.
Другой мембраностабилизирующий препарат — кетотифен — глазные капли также с успехом используют в лечении аллергического конъюнктивита. В двойном слепом рандомизированном исследовании уже через 15 мин и 2 часа спустя после его инстилляции у больных достоверно уменьшились проявления глазных симптомов, которые лучше контролировались, чем при приеме селективного антагониста Н1-рецепторов (эмедастин) [8]. Механизм действия кетотифена связан со стабилизацией мембран тучных клеток и уменьшением высвобождения из них гистамина, лейкотриенов и других медиаторов аллергии. Задитен — глазные капли 0,025% назначают взрослым и детям старше 12 лет по 1 капле 2 раза/сут в оба глаза. Длительность применения — не более 6 недель. Препарат в качестве консерванта содержит бензалкония хлорид, который способен проникать в материал мягких контактных линз, поэтому рекомендуется снимать линзы перед инстилляцией Задитен — глазные капли и надевать не ранее чем через 15 мин после инстилляции. Не следует применять Задитен — глазные капли при раздражении или воспалении глаз. В случае одновременного назначения с другими глазными каплями необходимо делать перерыв между инстилляциями не менее 5 мин.
Как перспективное средство терапии сезонных аллергических конъюнктивитов рассматривают топические нестероидные противовоспалительные препараты (глазные капли на основе диклофенака — Диклофенак-лонг, Наклоф, за рубежом широко используют Кеторолака трометамин 0,5%), механизм действия которых заключается в торможении активности арахидоновой кислоты. У этих препаратов отсутствуют те серьезные побочные эффекты, которые обычно присущи топическим кортикостероидам. В метаанализе восьми исследований, включавших 712 пациентов, после применения топических нестероидных противовоспалительных средств обнаружено статистически достоверное снижение выраженности кардинального симптома — зуда конъюнктивы глаз (p
Д. Ш. Мачарадзе, доктор медицинских наук, профессор
РУДН, Москва
Возможности противовоспалительной терапии больных полипозным риносинуситом
Независимо от причины, важнейший механизм развития и прогрессирования полипозного риносинусита — воспалительная реакция, нарушение функции мерцательного эпителия, вентиляции и дренажа околоносовых пазух. Лечение больных полипозным риносинуситом лежит глав
Regardless of the cause, the most important mechanism for the development and progression of polypous rhinosinusitis is an inflammatory reaction, a dysfunction of ciliary epithelium, ventilation and drainage of the paranasal sinuses. Treatment of patients with polypous rhinosinusitis lies mainly in the therapeutic plane, surgery is used only in the absence of the effect of drug. Intranasal glucocorticosteroids are used for all typical forms of bilateral polypous rhinosinusitis, they are the starting therapy for the initial stages of the disease without pronounced nasal obstruction and are prescribed by a long course.
Профилактика и лечение воспалительных заболеваний верхних отделов респираторного тракта остаются одной из наиболее актуальных и сложно решаемых проблем практического здравоохранения, несмотря на значительные успехи современной медицины. Воспалительная реакция лежит в основе многих хронических патологических состояний полости носа и околоносовых пазух, в том числе и такой нозологической формы, как полипозный риносинусит (ПРС). ПРС является одной из форм хронического риносинусита (ХРС) и, как правило, манифестирует в наиболее трудоспособном возрасте — 25–55 лет, мужчины страдают примерно в 2 раза чаще женщин. По результатам популяционных исследований, распространенность вышеуказанного заболевания возросла за последние десятилетия и в настоящее время варьирует от 1% до 4,3%. Проведенный в России эпидемиологический анализ выявил ПРС у 1–1,3% обследованных пациентов, то есть данной патологией в нашей стране может страдать до 1,5 млн человек [1–3]. Известно, что ПРС — опосредованное тимусзависимыми лимфоцитами-хелперами второго типа (Th2) воспаление слизистой оболочки носа и параназальных синусов невыясненной до настоящего времени этиологии. По определению международной консенсусной конференции EPOS-2012, полипозный риносинусит — это хроническое продуктивное Тh2-зависимое эозинофильное воспаление, которое приводит к ремоделированию слизистой оболочки носовой полости и околоносовых пазух с последующим формированием полипов [3]. Клетки Th2 вырабатывают интерлейкины, среди которых преобладают ИЛ-4, ИЛ-5, ИЛ-13, гранулоцитарно-макрофагальный колониестимулирующий фактор (ГМ-КСФ) и некоторые другие цитокины, что приводит к гиперпродукции антител разных классов, прежде всего IgE, пролиферации и дифференцировке В-лимфоцитов, индукции и усилению соответствующих видов воспаления [4, 5]. У некоторых пациентов хронический гнойный процесс в том или ином параназальном синусе может обусловливать инфильтрацию слизистой оболочки нейтрофилами и ее гиперплазию также с формированием полипов. В отличие от инфекционного ХРС с полипами, при полипозном риносинусите преобладает эозинофильное воспаление и патологический процесс практически всегда является двусторонним. Эозинофильная инфильтрация слизистой оболочки имеет место в среднем в 90% клинических случаев полипоза носа [2, 3].
Этиопатогенез ПРС до сих пор остается предметом дискуссий. На сегодняшний день в литературе указывается множество вероятных причин и механизмов формирования ПРС — наследственная предрасположенность, эозинофильное воспаление, IgE-зависимая аллергическая реакция, нарушение метаболизма арахидоновой кислоты, непереносимость нестероидных противовоспалительных средств, сенсибилизация к энтеротоксину золотистого стафилококка и другим бактериальным, грибковым, вирусным антигенам, наличие определенных изменений в околоносовых пазухах, нарушение аэродинамики полости носа и ряд других. До настоящего времени роль вышеуказанных факторов окончательно не определена, остается открытым вопрос, почему полипы образуются не у всех больных с имеющимися в анамнезе возможными причинами формирования ПРС. Не исключается мультифакторный аспект развития ПРС. Независимо от причины важнейший механизм развития и прогрессирования полипозного риносинусита — воспалительная реакция, нарушение функции мерцательного эпителия, вентиляции и дренажа околоносовых пазух [2, 3].
Очень важным с клинической точки зрения является коморбидность ПРС и бронхиальной астмы (БА). Полипозный риносинусит при БА обнаруживается у 7–15% больных, причем на фоне неаллергической астмы полипы определяются у 13%, а при аллергической природе астмы — в 5% случаев. Среди пациентов с ПРС астма диагностируется в 29–70% случаев. Часто ПРС наблюдается при аспириновой триаде — полипы в полости носа обнаруживаются у 36% пациентов с непереносимостью ацетилсалициловой кислоты [2, 6–8]. Не вызывает сомнений факт, что структурно и функционально верхний и нижний отделы дыхательного тракта представляют собой единое целое. Раздражение «астмагенных зон» полости носа постепенно увеличивающимися полипами и патологическим отделяемым приводит к усилению ринобронхиального рефлекса, что может вызывать функциональные нарушения бронхов, провоцирует развитие и поддерживает течение бронхиальной астмы и хронической обструктивной болезни легких. Современные данные о механизмах воспаления, роли аллергии в патогенезе и развитии заболевания, функциональной активности эозинофилов и провоспалительных цитокинов дополнили и углубили представления специалистов о этиопатогенезе ПРС и его взаимосвязях с бронхиальной астмой. Выявлена связь изменений показателей функции внешнего дыхания с нарастанием тяжести и распространенности воспаления в полости носа и околоносовых пазухах. БА, особенно среднетяжелого и тяжелого течения, значительно снижает социальную активность человека, в детском возрасте ограничивает физическое развитие, у взрослых является причиной значительного количества дней нетрудоспособности, часто обусловливает формирование таких патологических состояний, как дыхательная недостаточность, астматический статус, легочное сердце, эмфизема легких. С каждым годом, несмотря на прогресс современного здравоохранения, увеличивается число лиц со стойкой нетрудоспособностью на фоне данной патологии, ежегодно в мире от БА и ее осложнений погибает около четверти миллиона человек. Сочетание ПРС с бронхиальной астмой, особенно при присоединении инфекционного фактора, в перспективе приводит к более распространенным поражениям дыхательных путей. Широкая распространенность полипозного риносинусита и его частая ассоциация с БА обусловливают необходимость к таким пациентам междисциплинарного подхода с участием врачей различных специальностей — оториноларингологов, пульмонологов, аллергологов, терапевтов, педиатров и других [7, 9].
Клинически ПРС проявляется персистирующей назальной обструкцией, выделениями из носа слизистого характера, болью и ощущением давления в области лица, снижением обоняния или его потерей. Современная диагностика ПРС состоит из нескольких этапов — комплексной оценки жалоб пациента, анамнестических данных, включающих аллергоанамнез, наличие симптомов бронхиальной астмы и других коморбидных состояний, а также результатов лабораторных и инструментальных методов исследования. К инструментальным методам диагностики ПРС относится эндоскопический осмотр полости носа и носоглотки, а также рентгенологическое исследование — мультиспиральная (МСКТ) или конусно-лучевая (КЛКТ) компьютерная томография околоносовых пазух. МСКТ околоносовых пазух, выполненная в двух проекциях — аксиальной и саггитальной, является «золотым стандартом» диагностики патологического процесса в околоносовых пазухах, в том числе и полипозного риносинусита [2, 3].
Разработке методов эффективного лечения больных ПРС посвящено большое количество исследований в нашей стране и за рубежом. До сегодняшнего дня адекватное ведение пациентов с ПРС остается серьезной нерешенной проблемой — отсутствуют эффективные схемы лечения и ни один из существующих методов не позволяет контролировать симптомы заболевания более чем на 60%, характерны частые рецидивы после хирургического лечения. В Российской Федерации рекомендовано при начальных формах ПРС с небольшими отечными полипами в верхних отделах полости носа использовать местное консервативное лечение. Если полипы полностью блокируют носовые ходы, целесообразно начинать с хирургического вмешательства, а затем назначить топическую терапию. Значительный прогресс в хирургическом лечении ПРС достигнут благодаря внедрению в практику эндоскопической функциональной синус-хирургии (FESS), однако, как показали многолетние наблюдения, результат операции зависит не только от техники самой операции, но и от методики ведения таких пациентов до и после хирургического лечения. Необходимо помнить, что лечение полипозного риносинусита лежит главным образом в терапевтической плоскости, хирургия используется только в случае отсутствия эффекта от медикаментозного воздействия и развитии осложнений, а также для коррекции нарушений архитектоники носа [2, 3].
Ведущая роль воспаления в патогенезе ПРС обусловливает использование в лечении таких больных препаратов гормонов коры надпочечников — глюкокортикостероидов (ГКС) естественного и синтетического происхождения. ГКС системно в клинической практике используются с конца 1940-х годов. Мощный противовоспалительный эффект является неспецифическим действием данных лекарственных веществ. Необходимо учитывать, что системные стероиды обладают целым комплексом известных побочных эффектов, поэтому в терапии пациентов с ПРС их использование ограничено. Системно ГКС используются при рецидивах ПРС в короткие сроки, при наличии противопоказаний к хирургическому вмешательству, как предоперационная подготовка и в некоторых других ситуациях. Ингаляционные и топические формы ГКС были синтезированы только спустя 30 лет начала эры стероидной терапии. Появление топических ГКС с низкой биодоступностью обусловило широкие перспективы и возможности их применения в клинической практике. Топические ГКС имеют высокое сродство к рецепторам, обладают более выраженной противовоспалительной активностью, применяются в небольших дозах (примерно в 100 раз ниже), чем системные, оказывают минимальное системное действие. Из местных нежелательных эффектов у ряда больных на фоне использования интраназальных глюкокортикостероидов (ИнГКС) отмечаются сухость слизистой оболочки полости носа и носовые кровотечения, которые проходят, как правило, самостоятельно через несколько дней после отмены препарата. Анализ результатов проведенных контролируемых исследований, основанных на клинико-функциональных, эндоскопических и рентгенологических методах оценки, продемонстрировал высокую эффективность ИнГКС, а сравнение эффективности хирургического и медикаментозного лечения ПРС показало, что терапия ИнГКС может рассматриваться как альтернативный хирургическому метод ведения таких пациентов [2, 3]. Эволюция местных стероидов заключается в повышении их топической активности, снижении биодоступности, повышении комплаентности и удобства дозирования и расширении показаний [10]. Действие ИнГКС при ПРС обусловливает уменьшение привлечения воспалительных клеток (эозинофилов, тучных клеток, Т-лимфоцитов, нейтрофилов и др.) и снижение действия их медиаторов в очаге воспаления, ингибирование синтеза арахидоновой кислоты, простагландинов, лейкотриенов и таким образом уменьшают экстравазацию плазмы, отек и секрецию слизи. ИнГКС используются в лечении всех типичных форм двустороннего ПРС, являются стартовой терапией при начальных стадиях заболевания без выраженной назальной обструкции и назначаются длительным курсом — 6 месяцев и более. Помимо местного эффекта — восстановления носового дыхания и снижения назальной эозинофилии, терапия ИнГКС увеличивает эффект противоастматических препаратов, при сочетанной терапии для поддержания контролируемого течения БА требовались значительно меньшие дозы ингаляционных ГКС. Больным ПРС рекомендовано также максимально раннее начало или возобновление курса терапии ИнГКС после хирургического вмешательства [2, 3].
В настоящее время в нашей стране наиболее широко используются следующие топические глюкокортикостероиды — беклометазона дипропионат, будесонид, флутиказона пропионат, флутиказона фуроат и мометазона фуроат. Для терапии больных ПРС официально зарегистрированы только будесонид и мометазона фуроат. Противовоспалительная активность ИнГКС зависит от ряда факторов — степени сродства к глюкокортикостероидному рецептору, липофильности, вязкости; комплаентности пациента; удобства дозирующего устройства и способности больного правильно им пользоваться. Вопрос о преимуществах того или иного ИнГКС в купировании воспалительных процессов в полости носа и околоносовых пазухах до сих пор остается весьма дискутабельным. На настоящий момент доказано отсутствие какого-либо эффекта воздействия большинства ИнГКС на гипоталамо-гипофизарно-надпочечниковую систему человеческого организма, за исключением беклометазона дипропионата [11, 12].
Значимое место в арсенале врачей занимает ГКС для интраназального применения Тафен® назаль, действующим веществом которого является синтетический глюкокортикостероидный препарат будесонид, обладающий выраженным противовоспалительным, противоаллергическим действием. При применении в терапевтических дозах будесонида (Тафен® назаль) практически не оказывает резорбтивного действия, не обладает минералокортикоидной активностью, хорошо переносится при длительном лечении. Будесонид оказывает ингибирующее действие на высвобождение медиаторов воспалительной реакции, повышает синтез противовоспалительных белков, снижает количество тучных клеток и эозинофильных гранулоцитов, предупреждает краевое стояние нейтрофилов, положительно влияет на воспалительную экссудацию и продукцию цитокинов. Будесонид уменьшает высвобождение токсичных протеинов из эозинофилов, свободных радикалов из макрофагов и лимфокинов из лимфоцитов и замедляет связывание адгезивных молекул с клетками эндотелия, препятствуя таким образом притоку лейкоцитов к месту воспаления. Препарат увеличивает количество α-адренорецепторов на поверхности мембраны гладких мышечных клеток сосудов, повышая чувствительность к деконгестантам. Будесонид ингибирует активность фосфолипазы А2, что приводит к торможению синтеза простагландинов, лейкотриенов и фактора активации тромбоцитов, индуцирующих воспалительную реакцию. Будесонид также ингибирует синтез гистамина, что приводит к уменьшению его уровня в тучных клетках. Эффект применения будесонида отмечается на уже вторые-третьи сутки после начала лечения [13].
В системный кровоток попадает лишь около 20% введенной дозы будесонида. Системная биодоступность будесонида является низкой, так как более 90% абсорбировавшегося препарата инактивируется в процессе «первого прохождения» через печень. Глюкокортикоидная активность метаболитов будесонида не превышает 1% [13].
В стандартных исследованиях на моделях животных и in vitro установлено, что аффинность будесонида к специфическим рецепторам глюкокортикоидов в 200 раз больше таковой для кортизола, а местный противовоспалительный эффект больше в 1000 раз. При проведении исследований системной активности будесонида на животных установлено, что при подкожном введении эффект будесонида был в 40 раз сильнее, чем у кортизола, а при приеме внутрь — в 25 раз. Будесонид формирует внутриклеточное депо в дыхательных путях благодаря обратимой эстерификации. Данный ИнГКС имеет высокое сродство к глюкокортикоидным рецепторам и быстро метаболизируется в печени до продуктов, имеющих низкую биологическую активность. Конъюгаты будесонида с длинноцепочечными жирными кислотами (олеиновой, стеариновой, пальмитиновой, пальмитолеиновой) внутри клеток отличаются высокой липофильностью, превышающей другие ИнГКС [13–15]. При сравнении терапевтических индексов было показано, что из всех ИнГКС наибольшую оценку эффективности в баллах, как по отдельным параметрам, так и в общем, имеет будесонид [16].
Важно отметить безопасность длительного использования будесонида. В литературе приведены результаты длительного, в течение 5,5 лет, непрерывного, интраназального применения будесонида в дозе 200–400 мкг/сутки у 24 пациентов с круглогодичным аллергическим или неаллергическим ринитом — ни у одного больного не было выявлено ни гистопатологических изменений слизистой оболочки, ни влияния на гипоталамо-гипофизарную систему, ни отрицательной динамики в гемограмме [17].
В двойном слепом плацебо-контролируемом многоцентровом исследовании 167 пациентов с устойчивыми, независимо от приема антибиотиков, симптомами риносинусита также было подтверждено сочетание хорошей переносимости и высокой эффективности будесонида. Пациенты получали 128 мкг 2 раза в день (256 мкг/сутки) будесонида или плацебо в течение 4 месяцев. В конце лечения 43,1% пациентов, получавших будесонид, заявили о значительном или полном контроле над симптомами риносинусита, в группе плацебо — только 25,9% [18]. Особо следует отметить, что будесонид является единственным ИнГКС, эффективность и безопасность которого были подтверждены в значительном количестве исследований у детей в возрасте от 6 месяцев [19]. В исследовании 78 детей в возрасте от 5 до 15 лет с круглогодичным аллергическим ринитом, получавших интраназально будесонид 200 мкг 2 раза в день в течение 12 месяцев, у 43 детей терапия была продолжена (400 мкг в сутки) еще на год. Во время и после лечения не было выявлено никакого негативного влияния на костный метаболизм, минеральную плотность костной ткани и рост детей, а также на уровень кортизола по сравнению с контролем [20]. Высокая эффективность будесонида в сравнительно низкой дозировке — 128 мкг 1 раз в день у детей 6–16 лет также доказана результатами контролируемого клинического исследования [21]. Будесонид является единственным препаратом из числа ИнГКС, который по классификации Управления по контролю пищевых продуктов и лекарственных препаратов США (Food and Drug Administration, FDA) относится к категории B — препаратам, для которых нет доказательств риска применения при беременности.
Таким образом, эффективность и безопасность будесонида, продемонстрированная результатами ряда клинических исследований, а также наличие юридических оснований позволяют рекомендовать широкое использование данного лекарственного средства в лечении больных полипозным риносинуситом, в том числе при наличии коморбидных состояний.
Литература
ФГБОУ ВО Первый МГМУ им. И. М. Сеченова, Москва
Возможности противовоспалительной терапии больных полипозным риносинуситом/ В. М. Свистушкин, Г. Н. Никифорова, Д. М. Пшонкина.
Для цитирования: Лечащий врач №11/2017; Номера страниц в выпуске: 72-75
Теги: дыхательные пути, полипы, астма, коморбидность