при атрофическом гастрите можно принимать кардиомагнил
Проблемы безопасности при использовании препаратов ацетилсалициловой кислоты для профилактики сердечно-сосудистых осложнений
В настоящем обзоре представлены данные о проблемах назначения ацетилсалициловой кислоты в широкой клинической практике. Рассмотрены вопросы, касающиеся возможностей профилактики поражений желудочно-кишечного тракта.
This review present data on problems in using of acetilsalicylic in cardiovascular prevention. The questions concerning opportunities of prevention of defeats of a gastrointestinal path are considered.
Лечение низкими дозами ацетилсалициловой кислоты (АСК) (в монотерапии или в комбинации с другими антитромбоцитарными препаратами) на сегодняшний день является основой вторичной профилактики при ишемической болезни сердца. Длительная терапия низкими дозами АСК рекомендована больным со стабильной ишемической болезнью сердца, у пациентов, перенесших острый коронарный синдром с подъемом и без подъема сегмента ST, после реваскуляризации [1–3].
Применение низких доз АСК в первичной профилактике вызывает больше вопросов. Здесь, при определении показаний к назначению АСК, ключевое значение приобретает соотношение пользы от назначения препарата и риском, связанным с его использованием. В настоящее время рекомендации Европейского общества кардиологов и Европейского общества гипертонии предусматривают назначение АСК больным с высоким риском сердечно-сосудистых осложнений, а также при снижении функции почек при условии хорошего контроля за артериальным давлением (АД) [4]. Выделение именно этих групп больных базируется на результатах субанализа исследования HOT. В этом исследовании участвовало 18 750 больных с артериальной гипертензией (АГ). Одной из задач исследования было оценить эффективность для первичной профилактики терапии АСК в дозе 75 мг/сут. Было показано снижение риска всех сердечно-сосудистых событий на 15% и инфаркта миокарда на 36%. Однако риск кровотечений увеличивался в 1,65 раза. Субанализ показал наиболее значимую эффективность применения АСК у больных с уровнем креатинина выше 1,3 мг/дл, АД выше 180/107 мм рт. ст. и у больных с высоким и очень высоким риском сердечно-сосудистых событий. При этом в этих группах не наблюдается значимого увеличения риска кровотечений [5].
Метаанализ трех основных исследований (JPAD, POPADAD и ETDRS), где АСК использовалась в качестве средства первичной профилактики у больных с сахарным диабетом, показал снижение риска всех сердечно-сосудистых событий на 9%. Именно поэтому применение низких доз АСК у больных с диабетом должно базироваться на индивидуальной оценке риска. Соотношение риск/польза склоняется в сторону большей полезности лишь у больных с высоким дополнительным риском [6].
Хотя применение АСК в первичной профилактике показано только больным высокого риска, АСК остается наиболее часто назначаемым в рутинной практике антитромбоцитарным препаратом. При опросе пациентов двух семейных клиник Канады оказалось, что лица старше 50 лет в 39% случаев регулярно получают АСК, причем 53% пациентов получают АСК для первичной профилактики сердечно-сосудистых и 46% с целью вторичной профилактики. Частота назначения АСК возрастает с возрастом. В возрастной группе 50–59 лет АСК получают 24% пациентов, в возрасте 70–79 лет — 48%. С возрастом возрастает пропорция больных, получающих АСК для вторичной профилактики сердечно-сосудистых осложнений [7]. При анализе 131 050 электронных карт больных, наблюдавшихся врачами общей практики в США, в период с 2008 по 2011 год оказалось, что доля больных, получающих АСК в рамках первичной профилактики осложнений, растет, несмотря на то, что польза от назначения АСК всем больных с АГ, сахарным диабетом, дислипидемией не является доказанной [8]. Широкое применение АСК делает особенно актуальной задачу оценки риска осложнений антитромбоцитарной терапии и поиск возможных путей профилактики этих осложнений.
Влияние антитромбоцитарных препаратов на состояние желудочно-кишечного тракта
Ульцерогенное действие АСК складывается из прямого повреждающего действия кислоты на слизистую оболочку ЖКТ и воздействия на синтез простагландинов. В синтезе простагландинов участвует фермент циклооксигеназа 1-го типа (ЦОГ-1), которую и блокируют нестероидные противоспалительные средства (НПВС), в том числе и АСК. Простагландин Е2 улучшает микроциркуляцию стенки ЖКТ, стимулирует синтез слизи и бикарбонатов, являющихся основным защитным барьером слизистой оболочки, нейтрализующим действие пепсина, желчных кислот и соляной кислоты. В целом при популяционной оценке риска, связанного с приемом НПВС, оказалось, что прием низких доз АСК несет за собой даже несколько меньший риск кровотечений из ЖКТ, чем НПВС (5,5 и 6,1). Нужно отметить, что ульцерогенным эффектом обладают и селективные ингибиторы циклооксигеназы 2-го типа. Это связывают с недостаточной степенью селективности и некоторым остаточным воздействием на ЦОГ-1. АСК в дозах, использующихся в кардиологической практике (325 мг и менее), по ульцерогенному эффекту сопоставима с неселективными НПВС. На большой когорте из почти 3000 больных провели ретроспективную оценку частоты возникновения поражений ЖКТ у больных, получающих низкие дозы АСК, и больных, получающих терапию НПВС. 1103 больных получали лечение АСК, 1856 больных — НПВС. Частота развития поражений ЖКТ составила 2,54% и 0,27% соответственно. При этом более высокая частота развития эрозивно-язвенных поражений при лечении АСК связана, вероятно, с более высокой степенью подавления синтеза простагландинов Е2 при лечении даже низкими дозами ацетилсалициловой кислоты [9].
Наиболее высок риск осложнений в начале антитромбоцитарной терапии. В исследовании на 991 больном с ишемической болезнью сердца (ИБС) оценили риск язвенных кровотечений на фоне терапии низкими дозами АСК. Оказалось, что 45% осложнений приходятся на первый месяц терапии АСК, общая частота осложнений составила 1,5% в год [10].
Показано, что замена АСК на клопидогрель или другие антитромбоцитарные препараты не снижает риска больших кровотечений [11]. По данным некоторых исследований с проведением эндоскопического контроля среди больных, имеющих симптомы диспепсии, на фоне применения клопидогреля тяжесть поражений ЖКТ и выраженность геморрагических проявлений выше, чем у больных, принимающих АСК [12].
Сочетанное применения АСК и НПВС существенно увеличивает риск кровотечений из ЖКТ и язвенных осложнений. Так, показано, что частота госпитализаций увеличивается с 0,6% в год при лечении низкими дозами, а до 1,5 в год при терапии и АСК и другими НПВС. Соответственно возрастает и потребность в применении профилактической терапии. Комбинация низких доз АСК с антикоагулянтами также приводит к 2-кратному увеличению риска осложнений.
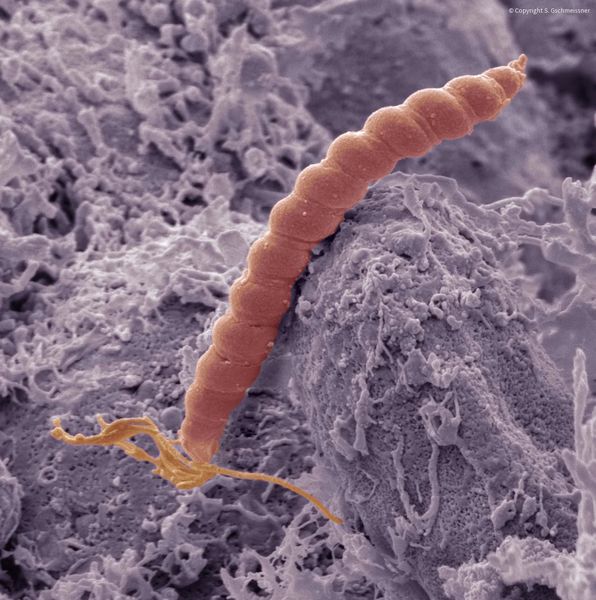
Инфекция Helicobacter pylori (Hp) также является наиболее значимым фактором, ассоциированным с развитием осложненных и неосложненных язвенных поражений как желудка, так и двенадцатиперстной кишки. При наличии Нр-инфекции риск кровотечений из верхних отделов ЖКТ возрастает в 4,9 раза и на фоне низких доз АСК и на фоне НПВС [13].
С практической точки зрения выделяют группы с низким, умеренным и высоким риском желудочно-кишечных кровотечений. Больные в возрасте моложе 65 лет и не имеющие дополнительных факторов риска имеют низкую вероятность развития кровотечений. Риск считается умеренным у больных старше 65 лет, при использовании НПВС, антиагрегатнов, бифосфонатов, блокаторов обратного захвата серотонина или кортикостероидов. Высокий риск кровотечений у больных, уже переносивших ЖКК или имеющих пептическую язву в анамнезе, а также у больных, получающих антикоагулянты. У больных с низким риском кровотечений специальной профилактики при использовании низких доз АСК не требуется. Больные умеренного или высокого риска кровотечений требуют дополнительных профилактических мероприятий.
Возможные подходы к профилактике поражений ЖКТ
К мерам профилактики желудочно-кишечных кровотечений и поражений ЖКТ при использовании АСК относится использование рациональных и обоснованных доз антитромбоцитарных препаратов, использование «защищенных» форм АСК, применение антацидов, блокаторов секреции и эрадикационная терапия.
Прием любых дозировок АСК сопровождается увеличением риска поражений ЖКТ, однако повышение риска коррелирует с принимаемой дозой АСК. В одном из исследований проанализировали риск кровотечений у больных, получавших 75 мг, 150 мг и 300 мг АСК. Риск осложнений возрастал в 2,3, 3,3 и 3,9 раза соответственно. Риск кровотечений был максимальным в начале приема АСК. Существенное увеличение риска отмечалось при комбинировании АСК с другими НПВС [14].
В другом исследовании при анализе группы 12 562 больных при проведении анализа безопасности приема разных доз АСК было показано, что только применение дозировок 75–81 мг/сут является более безопасным, чем применение более высоких доз препарата. При этом основной антиагрегантный эффект мало зависит от применяемой дозы АСК [15].
Таким образом, предпочтительным является использование низких доз АСК. При этом доза АСК в 75 мг/сут обладает доказанной эффективностью в предотвращении риска неблагопритяных исходов.
«Защищенные» формы АСК
Другим подходом к профилактике поражений ЖКТ при лечении АСК является использование «защищенных» лекарственных форм АСК. К таким формам относят кишечно-растворимые и буферные, в которых АСК сочетается с невсасывающимися антацидами. Данные об эффективности и безопасности этих форм противоречивы.
АСК адсорбируется из желудка путем пассивной диффузии в негидролизованном виде. Условием этого является сохраненная кислая среда желудка, обеспечивающая низкую скорость гидролиза ацетилсалициловой кислоты. Это обеспечивает биодоступность АСК около 50%. При использовании кишечно-растворимых форм АСК, из которых ацетилсалициловая кислота высвобождается в тонком кишечнике, биодоступность может снижаться за счет гидролиза АСК с участием кишечных гидролаз и щелочной среды кишечника. Следствием этого является сниженная блокада образования тромбоксана А2 при использовании кишечно-растворимых форм по сравнению с обычными [16].
Показано, что применение кишечно-растворимых форм АСК не снижает существенно риск эрозивно-язвенных поражений ЖКТ, а растворимые шипучие формы АСК могут этот риск даже повышать. При эндоскопической оценке воздействия разных форм АСК (АСК с кишечно-растворимой оболочкой или буферных форм АСК) оказалось, что при использовании кишечно-растворимых форм существенно увеличивается частота развития эрозивных и язвенных поражения тонкого кишечника [17].
В исследовании на 1402 больных, получающих низкие дозы АСК, оказалось, что частота кровотечений одинакова, а риск развития анемии несколько выше при использовании кишечно-растворимых форм (2% и 0,3%) [18].
Использование буферных форм, содержащих невсасывающиеся антациды, существенно снижает повреждающий потенциал в отношении слизистой желудка, связанный с приемом препарата [19].
При сравнении влияния буферной и обычной формы АСК на слизистую оболочку желудка на группе из 24 здоровых волонтеров оказалось, что гиперемия и эрозирование слизистой чаще отмечались при использовании небуферной формы. Клиническая симптоматика, связанная с гастропатией, появлялась только в группе с небуферной формой АСК. Интересно, что в исследовании использовались очень высокие дозы АСК (800 мг для буферной формы, 500 мг для обычной) [20]. При сравнении параметров фармакокинентики буферной и простой формы АСК у здоровых добровольцев было показано, что биодоступность АСК существенно не отличается, площадь под кривой концентрации препаратов также оказалась идентичной. Применение буферных форм АСК позволяло быстрее достичь максимальной концентрации препарата в крови [21].
Нужно отметить, что есть и данные об увеличении частоты осложнений со стороны ЖКТ при использовании буферных форм АСК. Так, метаанализ разных форм АСК показал, что относительный риск развития осложнений со стороны ЖКТ при применении обычных, кишечно-растворимых и буферных форм АСК составляет 2,6, 2,4 и 5,3 [22]. Однако следует учесть, что большинство буферных форм содержит высокие дозы АКС.
Особенный интерес представляет собой фармакологическая форма, сочетающая малую дозу АСК (75 мг) и невсасывающийся антацид — гидроокись магния, — Кардиомагнил. Показано, что такая форма АСК не уступает по влиянию на агрегацию тромбоцитов АСК в незащищенных или кишечно-растворимых формах [23]. Частота геморрагических и язвенных поражений верхних отделов ЖКТ при этом на фоне использования Кардиомагнила меньше, чем при использовании кишечно-растворимой формы АСК [24].
Медикаментозная профилактика поражений ЖКТ при терапии АСК
Чаще всего для профилактики медикаментозно обусловленных поражений ЖКТ используются различные блокаторы желудочной секреции, антациды, синтетические аналоги простагландинов.
Наиболее эффективны и широко используются, особенно у больных с высоким риском кровотечений, препараты из группы ингибиторов протонной помпы (ИПП), применение которых эффективно снижает риск кровотечений. В большом когортном исследовании, проведенном в Японии, было показано, что увеличение частоты использования ИПП у больных, получающих НПВС и низкие дозы АСК, приводит к снижению частоты кровотечений из ЖКТ со 160 до 23,2/100 000 населения в год [25].
При проведении фармакоэкономического анализа было показано, что использование АСК в комбинации с ИПП практически в 2 раза уменьшает риск осложнений, связанных с кровотечениями из ЖКТ. Увеличивается продолжительность жизни при этих осложнениях (на 38 дней к году наблюдения, или на 61%). При этом увеличивается приверженность больных к терапии АСК (с 71% до 74%). Все это ведет к уменьшению риска повторных коронарных событий (на 26 в год на 10 000 больных) [26].
Еще один подход к профилактике желудочно-кишечных кровотечений связан с проведением эрадикации Hp-инфекции. Успешная эрадикация снижает риск кровотечений на фоне приема АСК в 5,5 раз [27]. Таким образом, больным с желудочно-кишечным кровотечением в анамнезе, при необходимости проведения антиагрегантной терапии, рекомендуется обследование для выявления Hp-инфекции и проведения эрадикационной терапии.
Таким образом, в настоящее время достаточно хорошо разработаны подходы к профилактике поражений ЖКТ при лечении АСК. Этот антитромбоцитарный препарат является одним из наиболее часто используемых в современной кардиологической и терапевтической практике. При этом особенно важно четко следовать показаниям к назначению АСК, применяя только в тех ситуациях, когда польза от назначения препарата превышает риск связанных с ним осложнений. Наиболее значимым для безопасного использования АСК является использование минимально эффективных доз препарата. Сочетание АСК с небольшими дозами антацидов может сделать применение АСК более безопасным, не влияя существенно на эффективность лекарства. Для больных с высоким риском кровотечений возможно также профилактическое использование блокаторов желудочной секреции, а при наличии показаний — проведение эрадикации Hp-инфекции.
Литература
Л. О. Минушкина, доктор медицинских наук, профессор
ФГБУ УНМЦ УД Президента РФ, Москва
Что такое атрофический гастрит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Жуковой М. А., гастроэнтеролога со стажем в 22 года.
Определение болезни. Причины заболевания
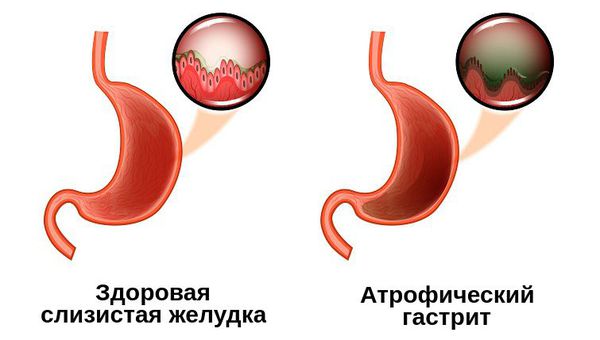
Атрофический гастрит — это наиболее коварный тип хронического гастрита, при котором изменяются париетальные клетки желудка, из-за чего слизистая оболочка становится тоньше, а железы желудка, вырабатывающие соляную кислоту, атрофируются. Это закономерно приводит к недостаточной выработке соляной кислоты и нарушению переваривания пищи.
Краткое содержание статьи — в видео:
Так как желудок является начальным звеном пищеварительной системы, нарушение его функции неизбежно влияет на состояние других органов: недостаточно переработанная в механическом и химическом отношении пища нарушает работу тонкого и толстого кишечника, а также поджелудочной железы.
Атрофический гастрит возникает и прогрессирует по разнообразным причинам, связанным с воздействием на слизистую оболочку желудка. Принято разделять их на две группы — экзогенные (внешние) и эндогенные (внутренние).
Существенными причинами появления заболевания также являются возрастные изменения: у людей до 30 лет атрофические процессы встречаются в 5 % случаев, до 50 лет — в 30 % случаев, после 50 лет — в 50-70 % случаев. Возможна и генетически обусловленная перестройка слизистой желудка по типу гипо- и атрофии.
Симптомы атрофического гастрита
Клиническая картина хронического гастрита связана с местными и общими расстройствами. Часто болезнь может протекать бессимптомно, особенно у людей после 50 лет. Симптомы, как правило, связаны с недостаточной работой желудка и зависят от степени поражения определённого звена пищеварения.
Основными функциями желудка являются:
При значительном снижении синтеза и отсутствии соляной кислоты возникают следующие местные проявления :
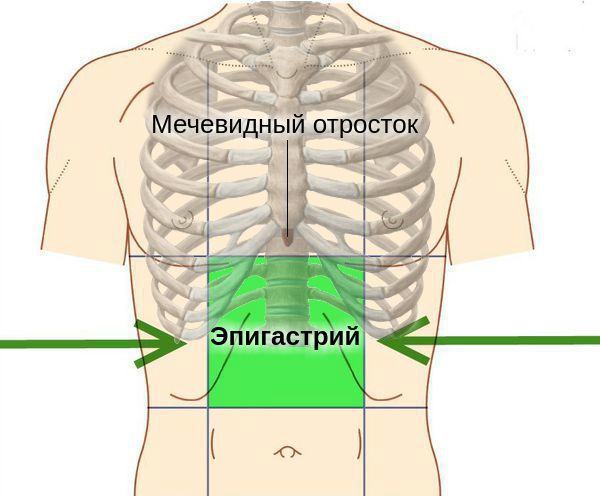
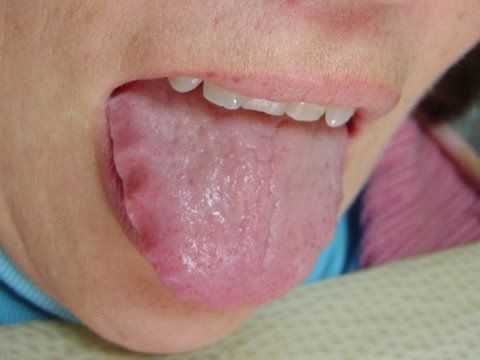
У людей с атрофическим гастритом отмечается «лакированный» язык, при обострениях язык увеличивается (видны отпечатки зубов), он обложен густым белым налётом. При пальпации (прощупывании) области желудка болезненность обычно отсутствует, но иногда возникает слабо выраженная разлитая болезненность в эпигастральной области.
У людей с аутоиммунным гастритом выявляются антитела к париетальным клеткам, сопутствует анемия, вызванная дефицитом витамина B12, и значительное снижение секреции соляной кислоты.
Симптомы общих расстройств:
Клинические симптомы гастрита нельзя сопоставить с гистологическими изменениями. Атрофический гастрит развивается медленно, поражение при этом начинается со дна желудка, переходя на его тело, а затем и на остальную слизистую. Считается, что на первых этапах умеренно выраженного атрофического гастрита клиника малосимптомная, стёртая и не имеет специфических проявлений. Но на дальнейших стадиях появляются симптомы, связанные с моторной и секреторной недостаточность желудка.
Патогенез атрофического гастрита
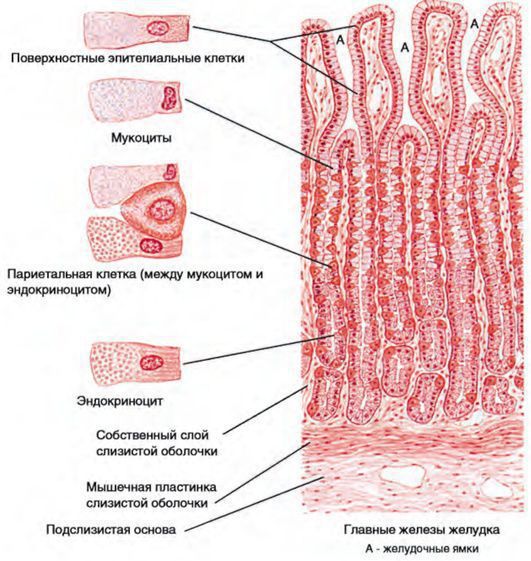
Эпителий слизистой оболочки желудка двухслойный:
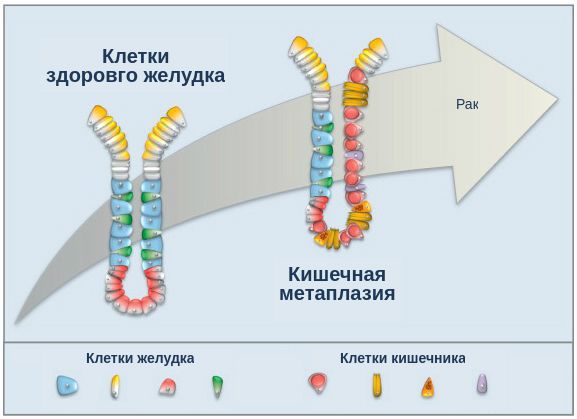
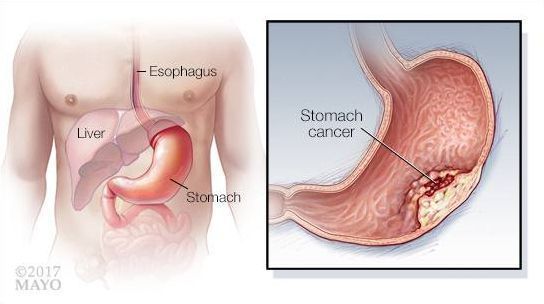
При гастрите оба слоя эпителия желудка вовлечены в патологический процесс. Заселение слизистой H. pylori вызывает хроническое повреждение клеток, ослабляет защитные свойства слизистой желудка, что ведёт к повреждению клеточных ядер свободными радикалами и токсинами. При этом изменяется клеточная структура, нарушается специализация клеток, появляются «гибридные» клетки, которые имеют свойства предраковых. Данный процесс называется кишечной метаплазией. В связи с этими изменениями слизистая желудка сначала приобретает вид тонкокишечного эпителия, затем — толстокишечного эпителия. Чем дальше заходит процесс метаплазии, тем больше вероятность развития аденокарциномы — железистого рака желудка.
Данный нарушенный процесс обновления клеток в слизистой желудка лежит в основе образования атрофии при гастрите. Прослеживается определённый патогенетический каскад, спровоцированный Н. pylori: от инфекционного гастрита через стадии атрофии, метаплазии и дисплазии к раку желудка. Особенно опасно появление неполной — толстокишечной — метаплазии.
Повреждение слизистой оболочки желудка при аутоиммунном гастрите реализуется через другой механизм: нарушение иммунитета приводит к образованию антител, повреждению ткани желудка иммунными комплексами. Чаще всего антитела вырабатываются к фактору Касла, который отвечает за всасывание витамина В12, и G-клеткам. Из-за этого постепенно снижается кислотность желудка, изменяется структура слизистой, снижается выработка соляной кислоты. В желудке нарушается всасывание железа и витаминов, развивается В12-дефицитная анемия. При этом заболевании в 90 % случаев выявляются антитела к париетальным клеткам, вырабатывающим соляную кислоту, и к Н + /К +- АТФазе, в 60 % случаев — антитела к фактору Касла.
Классификация и стадии развития атрофического гастрита
Сиднейская классификация гастритов
В последующем эта классификация дополнялась и уточнялась в связи с новыми научными данными. Сейчас для правильной формулировки диагноза «хронический гастрит» важно установить причину заболевания, распространённость поражения, степени активности и атрофии.
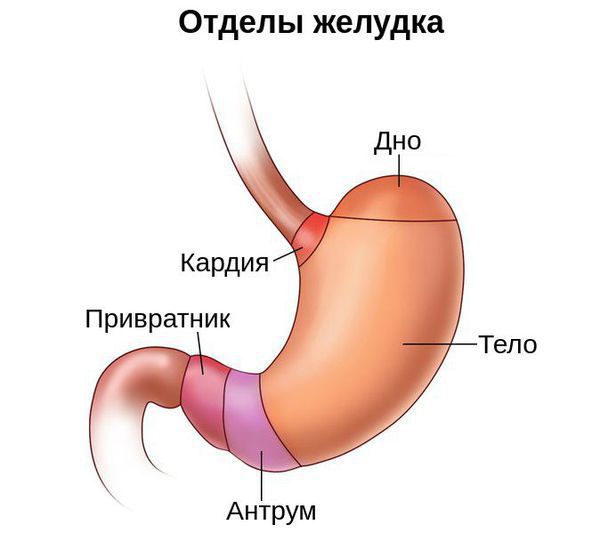
Условно желудок можно поделить на пять отделов: кардия, свод (дно, или фундальный отдел), тело, антрум и привратник. Атрофия может затронуть как один из этих отделов, так и весь желудок. В связи с этим выделяют диффузный атрофический гастрит (в фундальном, антральном или другом отделе) и мультифокальный атрофический гастрит (во всём желудке).
Морфологическая классификация гастрита широко применяется в практике, т. к. именно гистологические характеристики процесса помогают определить прогноз и тактику лечения пациента. Для этого используют визуально-аналоговую шкалу. Она позволяет оценить морфологическую картину слизистой желудка по:
Степень атрофии также оценивается по визуально-аналоговой шкале, изображённой на схеме ниже. По выраженности атрофии и её виду выделяют три категории изменений слизистой оболочки желудка:
При этом учитывается локализация и степень выраженности атрофических изменений (слабая, средняя, сильная), а также наличие и площадь очагов кишечной метаплазии.
Развитие болезни проходит определённые стадии:
Осложнения атрофического гастрита
Выраженный атрофический гастрит всегда сопровождается В12-дефицитной анемией, при которой париетальные клетки, вырабатывающие соляную кислоту, практически отсутствуют. Витамин В12, поступающий с пищей, не всасывается, что приводит к хронической анемии с характерными проявлениями в виде быстрой утомляемости, нарушения зрения и вкусовых ощущений, мышечной слабости, головокружений, чувства покалывания и онемения в конечностях.
При ахлоргидрии — отсутствии соляной кислоты в желудочном соке — происходит к выраженное нарушение пищеварения, ухудшается переработка пищи, снижается всасывание отдельных микроэлементов и витаминов.
Диагностика атрофического гастрита
Гастрит — диагноз морфологический, т. е. он основан не на симптомах, а на изменениях строения слизистой желудка. Поэтому он может считаться объективным только после оценки слизистой желудка, взятой во время биопсии. Этим занимается патоморфолог. Только с помощью морфологического исследования можно достоверно выявить атрофию, воспаление и деструкцию слизистой желудка.
Клинический диагноз гастрита, т. е. диагноз без морфологического исследования, практически не имеет смысла. Симптомы диспепсии, которые заставляют больного обратиться к врачу, носят лишь функциональный характер и не всегда указывают на те морфологические изменения, которые составляют суть гастрита.
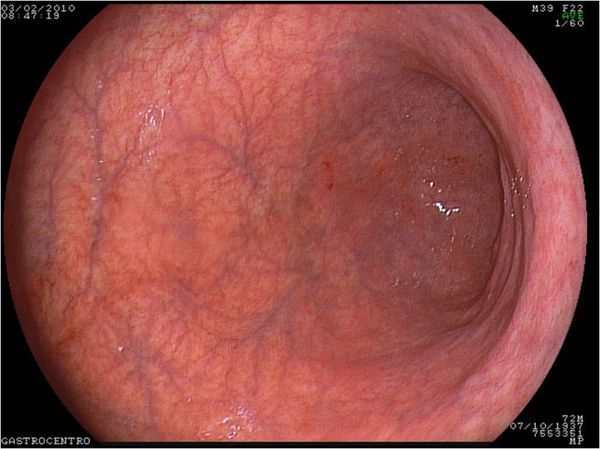
Изменения слизистой можно обнаружить при проведении эзофагогастродуоденоскопии (ЭГДС) — осмотре желудка и двенадцатиперстной кишки с помощью эндоскопа (через видео-трубку). Но результаты этого исследования являются субъективными и только косвенным образом могут указывать на наличие гастрита: они не позволяют оценить степень его прогрессирования.
Оптимальным методом является морфологическое исследование биоптатов. Также в практике широко используется быстрый уреазный тест — определение H. pylori методом оценки количества аммиака в мочевине, образуемого этими бактериями. К другим способам относятся дыхательный тест и иммуноферментные анализы.
Крайне важно провести диагностику Н. pylori до лечения и после уничтожения бактерий, чтобы контролировать эффективность выбранной схемы терапии. Это связано с появлением штаммов бактерий, устойчивых к антибиотикам.
Дефекты пищеварения хорошо выявляет анализ кала (микроскопическое исследование) — достаточно простой метод, который позволяет обнаружить косвенные признаки снижения выработки соляной кислоты, а также изменения, характерные для патологии других органов пищеварительной системы. Так, при атрофическом гастрите в кале появляется большое количество неизменённых мышечных волокон, перевариваемой клетчатки соединительной ткани и внутриклеточного крахмала.
Лечение атрофического гастрита
Современная терапия хронического гастрита предполагает воздействие на причины заболевания, в частности устранение H. pylori и лечение аутоиммунного гастрита.
Устранить аутоиммунные механизмы повреждения слизистой желудка можно только благодаря гормональной терапии. Назначение глюкокортикостероидов оправдано только при сопутствующей В12-дефицитной анемии.
Совершенно другой подход при обнаружении инфекции H. pylori и лабораторных подтверждений атрофических изменений. Он предполагает эрадикацию — уничтожение H. pylori. Терапия назначается после проведения суточной рН-метрии. При значении рН менее 6, несмотря на пониженную выработку соляной кислоты, назначаются ингибиторы протонной помпы (ИПП); при анацидном состоянии (рН ≥ 6) ИПП исключаются из схемы эрадикации и назначаются только антибиотики.
Через 4-6 недель после окончания антихеликобактерной терапии необходимо провести контрольное исследование — С13-уреазный дыхательный тест.
Хронический химикоиндуцированный или желчный рефлюкс-гастрит объединяет большую группу больных, включая:
Цель лечения — нормализовать моторику желудочно-кишечного тракта и связывание желчных кислот.
Тактика лечения зависит от основной причины гастрита:
Прогноз. Профилактика
Прогноз заболевания серьёзнее у пациентов старше 50 лет, т. к. в этом возрасте метапластические процессы развиваются гораздо быстрее и чаще приводят к появлению рака. Эффективность лечения зависит от степени выраженности атрофии и площади поражения. Большое значение имеет ранее начало лечения и полное устранение H. pylori. При выявлении инфекции после проведения терапии необходимо повторное лечение.
Предраковые изменения на фоне атрофического гастрита (кишечная метаплазия и дисплазия) представляют наибольшую опасность. При этом своевременная диагностика и полное удаление H. pylori уже через пять лет восстанавливают слизистую желудка и значительно уменьшают площадь метаплазии.