Рецепт ацетилхолина на латыни
Ацетилхолин
Действующее вещество (международное непатентованное название)
Русское название: Ацетилхолин
Латинское название: Acetylcholine
Химическое название.
Характеристика.
Ацетилхолина хлорид — бесцветные кристаллы или белая кристаллическая масса. Расплывается на воздухе. Легко растворим в воде, хлороформе и этаноле; практически нерастворим в эфире.
Фармакология.
Осуществляет передачу нервных импульсов в ЦНС, вегетативных ганглиях, окончаниях парасимпатических и двигательных нервов, возбуждает постсинаптические мембраны потовых желез. Взаимодействует с м- и н-холинорецепторами, вызывает деполяризацию мембраны, повышает проницаемость для ионов натрия, выравнивая потенциал напряжения. Стимуляция м-холинорецепторов увеличивает содержание «вторичных медиаторов» (цАМФ и цГМФ). Локальный синаптический потенциал генерирует потенциал действия в нейроне следующей ступени или повышает функциональную активность клеток органов (мышцы, железы и др.).
При системном действии преобладают м-холиномиметические эффекты: брадикардия, расширение кровеносных сосудов, снижение АД, повышение тонуса и сократимости гладких мышц бронхов, ЖКТ, матки, желчного и мочевого пузыря, усиление секреции пищеварительных, бронхиальных, потовых и слезных желез, сужение зрачков (миоз), спазм аккомодации. Снижает внутриглазное давление (при сужении зрачка и уплощении радужной оболочки расширяются шлеммов канал и пространства радужно-роговичного угла, улучшается отток внутриглазной жидкости). Стимулирующее влияние на н-холинорецепторы вегетативных ганглиев (симпатических и парасимпатических) значимо проявляется только при блокаде м-холинорецепторов.
При приеме внутрь неэффективен, т.к. легко гидролизуется; в условиях парентерального введения оказывает быстрый, но кратковременный эффект. После аппликации в конъюнктивальный мешок всасывается в кровь, оказывает резорбтивное действие. Плохо проникает через ГЭБ.
Показания.
Операции на передней камере глаза (удаление катаракты, кератопластика, иридоэктомия) — для обеспечения миоза в течение нескольких секунд после высвобождения хрусталика; спазм артерий сетчатки; редко — эндартериит, перемежающаяся хромота, трофические расстройства в культях, атония кишечника и мочевого пузыря, рентгенодиагностика ахалазии пищевода.
Противопоказания.
Гиперчувствительность, бронхиальная астма, хроническая сердечная недостаточность II–III ст., стенокардия, атеросклероз, эпилепсия, кровотечения из ЖКТ.
Побочные действия.
При системном применении или системной абсорбции: сужение коронарных сосудов, брадикардия, аритмия, снижение АД, покраснение лица, затруднение дыхания, повышенное потоотделение.
При аппликации в глаза: отек, помутнение роговицы.
Взаимодействие.
Проявляет антагонизм с адреномиметиками по влиянию на величину зрачка. Бета-адреноблокаторы, антихолинэстеразные препараты, адреномиметики повышают противоглаукомный эффект. Трициклические антидепрессанты, м-холиноблокаторы, фенотиазин, хлорпротиксен, клозапин снижают парасимпатическую активность. Галотан усиливает побочные проявления. При сочетании с хинидином возможно трепетание желудочков.
Способ применения и дозы.
Местно: равномерно нанося на поверхность радужной оболочки и в направлении к углу зрачка 0,5–2 мл.
Парентерально: по 0,05–0,1 г п/к или в/м 1–3 раза в сутки. Высшие дозы п/к и в/м: разовая — 0,1 г, суточная — 0,3 г.
Передозировка.
Симптомы: резкое снижение АД, брадикардия, нарушение ритма сердца, профузный пот, миоз, усиление перистальтики кишечника, бронхоспазм, остановка сердца.
Лечение: немедленное в/в, п/к или в/м введение 0,5–1 мл 0,1% раствора атропина (при необходимости повторно), при тяжелом бронхоспазме и резком падении АД — 0,1–1 мл 0,1% раствора адреналина п/к.
Применение при беременности и кормлении грудью.
Категория действия на плод по FDA — C.
Меры предосторожности.
Раствор готовят непосредственно перед использованием, т.к. ацетилхолин в растворе быстро разлагается.
При инъекции следует убедиться, что игла не попала в вену: в/в введение не допускается (возможно резкое понижение АД и остановка сердца).
Длительная аппликация (в течение нескольких лет) в конъюнктивальный мешок может привести к необратимому миозу и образованию задних петехий.
Для пролонгации миоза возможна предварительная инстилляция пилокарпина. При операции по поводу катаракты применяют только после выделения хрусталика.
АЦЕТИЛХОЛИН
АЦЕТИЛХОЛИН — медиатор нервного возбуждения. Синтезируется в организме из аминоспирта холина и уксусной кислоты. Биологически очень активное вещество.
Ацетилхолин оказывает многостороннее действие на организм. Основная функция — медиация нервных импульсов. Нервные волокна и соответствующие им нейроны, осуществляющие передачу нервных импульсов посредством ацетилхолина, называются холинергическими. К ним относятся мотонейроны, иннервирующие скелетные мышцы; преганглионарные нейроны парасимпатических и симпатических нервов; постганглионарные нейроны всех парасимпатических и некоторых симпатических нервов (матки, потовых желез) и некоторые нейроны центральной нервной системы. Все холинергические волокна содержат холинацетилтрансферазу — специфический фермент, с помощью которого происходит синтез ацетилхолина. Ацетилхолин находится в нервных окончаниях в пузырьках, из которых он изливается в синаптическую щель в момент прихода нервного импульса. Освобождение ацетилхолина нервными окончаниями носит квантовый характер. По-видимому, содержимое пузырька и составляет ту наименьшую порцию ацетилхолина (квант), которая может быть выделена. В нормальных условиях каждый нервный импульс вызывает выделение нескольких сотен квантов ацетилхолина. Взаимодействуя со специфической макромолекулой на постсинаптической мембране — холинорецептором, ацетилхолин повышает проницаемость мембраны для ионов: возникает постсинаптический потенциал, который изменяет возбудимость эффекторной клетки, а в случае нервно-мышечного синапса является непосредственной причиной генерации потенциала действия. Эффект ацетилхолина прекращается под влиянием фермента ацетилхолинэстеразы (см. Холинэстеразы), который гидролизует ацетилхолин на малоактивный холин и уксусную кислоту, а также вследствие простой диффузии ацетилхолина из синаптической щели. В молекуле ацетилхолина есть две активные группы, обеспечивающие взаимодействие с холинорецептором: заряженная триметиламмониевая группа (катионная «головка»), которая реагирует с анионной группой в холинорецепторе, и сильно поляризованная сложноэфирная группа, реагирующая с так называемым эстерофильным участком холинорецептора.
В обычных условиях преобладает мускариноподобное действие ацетилхолина. При инстилляции ацетилхолина в глаз происходит сужение зрачка и спазм аккомодации, снижается внутриглазное давление. При попадании в общий кровоток наблюдается снижение кровяного давления, вызванное расширением сосудов (коронарные сосуды человека ацетилхолин суживает) и в меньшей степени замедлением сердечной деятельности, усиление двигательной активности желудочно-кишечного тракта, сокращение мускулатуры бронхов, желчного и мочевого пузыря, матки, усиление секреции желез с холинергической иннервацией, особенно слюнных и потовых.
Никотиноподобное действие ацетилхолина на вегетативные ганглии и надпочечники проявляется после атропинизации и при использовании более высоких доз. Оно выражается в прессорном эффекте. Ацетилхолин также стимулирует никотиночувствительные системы каротидных клубочков и рефлекторно возбуждает дыхание.
Все эффекты ацетилхолина можно усилить путем предварительного введения антихолинэстеразных веществ (эзерин, прозерин и др.). При обычных путях введения ацетилхолин не проникает через гемато-энцефалический барьер и не оказывает влияния на центральную нервную систему. Многообразие эффектов ацетилхолина, среди которых могут оказаться нежелательные, ослабляющие друг друга, а также кратковременность действия крайне ограничивают его применение в медицинской практике. Ацетилхолин широко используют при экспериментальном исследовании функций холинергических структур в виде хорошо растворимой соли — ацетилхолина хлорида (Acetylcholini chloridum, Acetylcholinum chloratum; список Б). Форма выпуска: ампулы по 5 мл, содержащие 0,2 г препарата.
Ацетилхолин как медиатор аллергических реакций
Сходство картины отравления ацетилхолином у собак с картиной развития у них анафилактического шока (см.) позволило предположить непосредственное участие холинергических процессов, имеющих место в деятельности некоторых органов, в механизме аллергических реакций этих органов. Таким органом является, напр., язык собаки, имеющий парасимпатическую иннервацию. Предполагалось, что точкой приложения антигена в сенсибилизированном органе служат окончания парасимпатических нервов. Это было подтверждено экспериментально. Введение антигена в сосуды языка сенсибилизированной собаке вызывает явный сосудорасширяющий эффект. В норме эти явления не наблюдаются. При выключении парасимпатической иннервации половины языка путем предварительного (за месяц до опыта) вылущения подчелюстной и подъязычных слюнных желез и вместе с ними подчелюстных и подъязычных периферических узлов парасимпатического иннервационного аппарата сосудов языка собаки полностью снимается описанная выше реакция сосудов этой половины языка на антиген. Вместе с тем при перерезке язычного нерва характер сосудистой реакции на антиген не меняется, что свидетельствует об отсутствии реакции на антиген чувствительных окончаний соматических нервов. Участие ацетилхолина в процессах распространения отравления в организме маловероятно. Роль анафилактического яда в этом смысле выполняют, очевидно, более стойкие продукты распада ткани, к которым относятся активные кинины, серотонин, гистамин и др. Таким образом, ацетилхолиновая гипотеза патогенеза аллергии ни в какой степени не противоречит представлению об участии гистамина в качестве одного из важных звеньев в механизме аллергической альтерации ткани. Участие ацетилхолина и холинергических процессов в механизме «органной» аллергии, то есть в условиях его действия in loco nascendi в соответствующих холинергических синапсах, имеет значение существенного, а в ряде структур и основного звена в определении функциональных выражений аллергии. К таким структурам относятся синаптические связи в вегетативной и центральной нервной системе, парасимпатическая сосудодвигательная иннервация, иннервация сердца и т. д. Вероятно, в них изменяется активность холинэстеразы, увеличивается скорость освобождения ацетилхолина при возбуждении их специфическим антигеном и, что самое важное, в них появляется возбудимость к специфическому антигену, который совершенно или почти совершенно отсутствовал в нормальном состоянии.
Библиография: Аничков С. В. и Гребенкина М. А. Фармакологическая характеристика холинорецепторов центральной нервной системы, Бюлл. эксперим. биол, и мед., т. 22, № 3, с. 28, 1946; Кибяков А. В. Химическая передача нервного возбуждения, М.— Л., 1964, библиогр.; Михельсон М. Я. и Зеймаль Э.В. Ацетилхолин, о молекулярном механизме действия, Л., 1970, библиогр.; Руководство по фармакологии, под ред. Н. В. Лазарева, т. 1, с. 137, Л., 1961; Турпаев Т. М. Медиаторная функция ацетилхолина и природа холино-рецептора, М., 1962; Э к к л с Д. Физиология синапсов, пер. с англ., М., 1966, библиогр.; Central cholinergic transmission and its behavioral aspects, Fed. Proc., v. 28, p. 89, 1969, bibliogr.; Dale H.H. The action of certain esters and ethers of choline, and their relation to muscarine, J. Pharmacol., v. 6, p. 147, 1914; Goodman L. S. a. G i 1 m a n A. Pharmacological basis of therapeutics, N. Y., 1970; Katz B. The release of neural transmitter substances, Springfield, 1969, bibliogr.; Michelson M. J. a. Danilov A. F. Cholinergic transmissions, в кн.: Fundament. biochem. Pharmacol., ed. by Z. M. Bacq, p. 221, Oxford a. o., 1971.
H. Я. Лукомская, М. Я. Михельсон; А. Д. Адо (алл.).
Ацетилхолин
Фармакологическое действие
Ацетилхолин оказывает холиномиметическое действие.
Фармакодинамика
Ацетилхолин является м-, н-холиномиметиком.
Осуществляет передачу нервных импульсов в центральной нервной системе, вегетативных ганглиях, окончаниях парасимпатических и двигательных нервов, возбуждает постсинаптические мембраны потовых желёз. Взаимодействует с м- и н-холинорецепторами, вызывает деполяризацию мембраны, повышает проницаемость для ионов натрия, выравнивая потенциал напряжения. Стимуляция м-холинорецепторов увеличивает содержание «вторичных медиаторов» (цАМФ и цГМФ). Локальный синаптический потенциал генерирует потенциал действия в нейроне следующей ступени или повышает функциональную активность клеток органов (мышцы, железы и др.). Участвует в передаче нервного импульса в разных отделах мозга, при этом малых концентрациях облегчает, а в высоких — тормозит синаптическую передачу.
При системном действии преобладают м-холиномиметические проявления брадикардия, уменьшение общего периферического сосудистого сопротивления, снижение артериального давления, повышение тонуса и сократимости гладких мышц бронхов, желудочно-кишечного тракта, матки, желчного и мочевого пузыря, усиление секреции пищеварительных, бронхиальных, потовых и слёзных желёз, сужение зрачков (миоз), спазм аккомодации.
Сужение зрачка, обусловленное действием ацетилхолина, как правило сопровождается снижением внутриглазного давления. Этот эффект частично объясняется тем, что при сужении зрачка и уплощении радужной оболочки расширяется шлеммов канал (венозный синус склеры) и фонтановы пространства (пространства радужно-роговичного угла), что обеспечивает лучший отток жидкости из внутренних сред глаза. Не исключено, что в понижении внутриглазного давления принимают участие и другие механизмы. Стимулирующее влияние на н-холинорецепторы вегетативных ганглиев (симпатических и парасимпатических) значимо проявляется только при блокаде м-холинорецепторов.
При приёме внутрь ацетилхолин неэффективен, так как легко гидролизуется; в условиях парентерального введения оказывает быстрый, но непродолжительный эффект. После аппликации в конъюнктивальный мешок всасывается в кровь, оказывает резорбтивное действие.
Фармакокинетика
Ацетилхолин показывает низкую абсорбцию. Плохо проникает через гематоэнцефалический барьер.
Показания
Противопоказания
Беременность и грудное вскармливание
Рекомендуется избегать применения ацетилхолина при беременности и в период лактации.
Способ применения и дозы
Подкожно и внутримышечно в дозе 50–100 мг 2–3 раза в сутки.
Максимальная разовая доза — 100 мг.
Максимальная суточная доза — 300 мг.
Побочные действия
При системном применении или системной абсорбции
Аллергические реакции, сужение коронарных сосудов, снижение артериального давления, брадикардия, аритмии, гиперемия кожи лица, затруднение дыхания, повышенное потоотделение, миоз, диарея, усиление перистальтики кишечника.
При аппликации в глаза
Отёк, помутнение роговицы.
Передозировка
Симптомы передозировки ацетилхолином
брадикардия, профузный пот, галлюцинации, коллапс, миоз, бронхоспазм, остановка сердца
Лечение передозировки ацетилхолином
Внутривенно или подкожно, 1 мл 0,1 % раствора атропина, при тяжёлом бронхоспазме и резком снижении артериального давления — 0,1–1 мл 0,1 % раствора эпинефрина подкожно.
Взаимодействие
Ацетилхолин показывает антагонизм с адреномиметиками по влиянию на величину зрачка.
Бета-адреноблокаторы, антихолинэстеразные препараты, адреномиметики при сочетании с ацетилхолином повышают противоглаукомный эффект.
При одновременном применении трициклические антидепрессанты, м-холиноблокаторы, фенотиазин, хлорпротиксен, клозапин снижают парасимпатическую активность.
При одновременном применении галотан усиливает побочные проявления.
При сочетании ацетилхолина с хинидином возможно трепетание желудочков.
Особые указания
Раствор готовят непосредственно перед использованием, так как при кипячении и длительном хранении растворы разлагаются.
Во время проведения инъекции необходимо убедиться, что игла не попала в вену (внутривенное введение не допускается из-за возможности резкого снижения артериального давления и остановки сердца).
Длительная аппликация (в течение нескольких лет) в конъюнктивальный мешок может привести к необратимому миозу и образованию задних петехий.
Для пролонгации миотического действия возможна предварительная инстилляция пилокарпина.
При операции по поводу катаракты применяют только после выделения хрусталика.
Молекула здравого ума
Автор
Редактор
Ацетилхолин — не самое знаменитое вещество, но он играет важную роль в таких процессах, как память и обучение. Давайте приоткроем завесу тайны над одним из самых недооцененных нейромедиаторов нашей нервной системы.
Первый среди равных
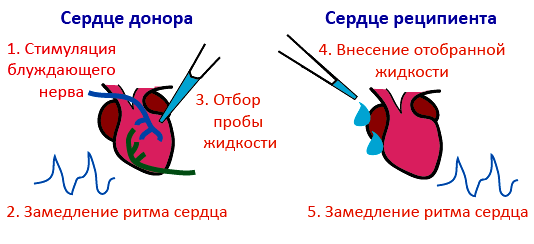
Рисунок 1. Классический опыт Отто Лёви по выявлению химических посредников передачи нервных импульсов (1921 год). Объекты — изолированные и погруженные в солевой раствор сердцá двух лягушек (донора и реципиента). Описание приведено в тексте. Рисунок с сайта en.wikipedia.org, адаптирован.
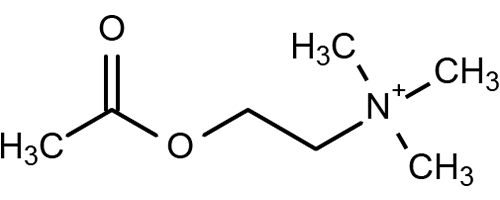
Рисунок 2. Структурная формула ацетилхолина. Рисунок с сайта www.curezone.org.
В научно-популярной литературе медицинской и нейрофизиологической направленности чаще всего речь заходит о трех нейромедиаторах: дофамине [1], серотонине [2] и норадреналине [3]. Во многом это объясняется тем, что нормальные и болезненные состояния, связанные с изменением уровня этих нейротрансмиттеров, доступнее для понимания и вызывают больше интереса у читателей. Об этих веществах я уже писал, теперь настало время уделить внимание еще одному медиатору.
Речь пойдет об ацетилхолине, и это будет символично, учитывая, что он был первым открытым нейромедиатором. В начале XX века между учеными велся спор, каким способом передается сигнал от одной нервной клетки на другую. Одни считали, что электрический заряд, пробежав по одному нервному волокну, передается на другое по каким-то более тонким «проводам». Их оппоненты утверждали, что существуют вещества, которые переносят сигнал от одной нервной клетки к другой. В принципе, обе стороны оказались правы: существуют химические и электрические синапсы. Однако сторонники второй гипотезы оказались «правее» — химические синапсы преобладают в организме человека.
Чтобы разобраться в особенностях передачи сигнала от одной клетки к другой, физиолог Отто Лёви проводил простые, но изящные опыты (рис. 1). Он стимулировал электрическим током блуждающий нерв лягушки, что приводило к уменьшению частоты сердечных сокращений*. Затем жидкость, находящуюся вокруг этого сердца, Лёви собирал и наносил на сердце другой лягушки — и оно тоже замедлялось. Это доказывало существование некоего вещества, передающего сигнал от одних нервных клеток другим. Загадочное вещество Лёви назвал vagusstoff («вещество блуждающего нерва»). Сейчас мы знаем его под названием ацетилхолин. Вопросом химической синаптической передачи занимался и британец Генри Дейл, который обнаружил ацетилхолин еще раньше Лёви. В 1936 году оба ученых получили Нобелевскую премию по физиологии и медицине «за открытия, связанные с химической передачей нервных импульсов».
* — О том, как сокращается наше сердце — об автоматизме, дирижирующих пейсмейкерах и даже смешных каналах, — читайте в обзоре «Метроном: как руководить разрядами?» [4]. — Ред.
Ацетилхолин (рис. 2) производится в нервных клетках из холина и ацетилкофермента-А (ацетил-КоА). За разрушение ацетилхолина отвечает фермент ацетилхолинэстераза, находящийся в синаптической щели; об этом ферменте будет подробный разговор позже. План строения ацетилхолинергической системы головного мозга схож со строением других нейромедиаторных систем (рис. 3). В стволе мозга существует ряд структур, выделяющих ацетилхолин, который поступает по аксонам в базальные ганглии головного мозга. Там есть свои ацетилхолиновые нейроны, чьи отростки расходятся широко по коре и проникают в гиппокамп.
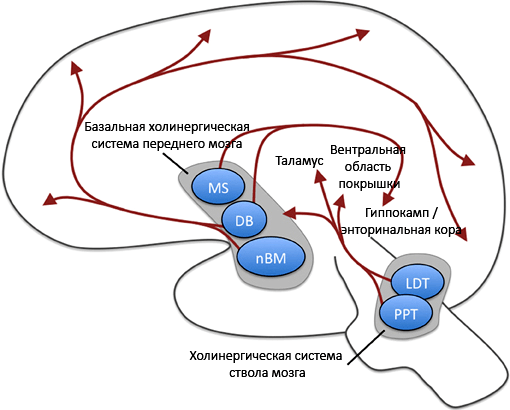
Рисунок 3. Ацетилхолиновая система мозга. Мы видим, что в глубоких отделах головного мозга находятся скопления нервных клеток (в переднем мозге и стволе), которые посылают свои отростки в различные отделы коры и подкорковых областей. В конечных пунктах из нейронных окончаний выделяется ацетилхолин. Местные эффекты нейромедиатора различаются в зависимости от типа рецептора и его расположения. MS — медиальное ядро перегородки, DB — диагональная связка Брока, nBM — базальное магноцеллюлярное ядро (ядро Мейтнера); PPT — педункулопонтийное тегментальное ядро, LDT — латеральное дорсальное тегментальное ядро (оба ядра — в ретикулярной формации ствола мозга). Рисунок из [8], адаптирован.
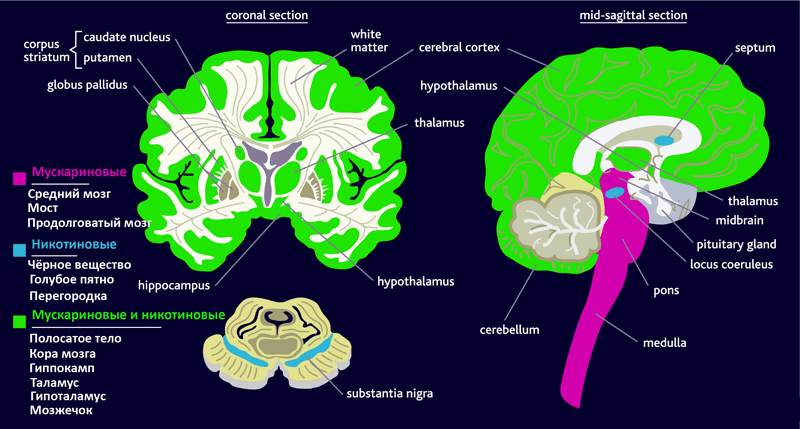
Рецепторы ацетилхолина делятся на две группы — мускариновые и никотиновые. Стимуляция мускариновых рецепторов приводит к изменению метаболизма в клетке через систему G-белков* (метаботропные рецепторы), а воздействие на никотиновые — к изменению мембранного потенциала (ионотропные рецепторы). Это происходит благодаря тому, что никотиновые рецепторы связаны с натриевыми каналами на поверхности клеток. Экспрессия рецепторов различается в разных участках нервной системы (рис. 4).
* — О пространственных структурах нескольких представителей громадного семейства GPCR-рецепторов — мембранных рецепторов, действующих через активацию G-белка, — доступно рассказано в статьях: «Рецепторы в активной форме» (об активной форме родопсина) [5], «Структуры рецепторов GPCR „в копилку“» (о дофаминовом и хемокиновом рецепторах) [6], «Рецептор медиатора настроения» (о двух серотониновых рецепторах) [7]. — Ред.
Рисунок 4. Распределение мускариновых и никотиновых рецепторов в головном мозге человека. Рисунок с сайта www.cnsforum.com, адаптирован.
Медиатор памяти и обучения
Ацетилхолиновая система головного мозга напрямую связана с таким явлением как синаптическая пластичность — способность синапса усиливать или снижать выделение нейромедиатора в ответ на увеличение или уменьшение его активности. Синаптическая пластичность является важным процессом для памяти и обучения, поэтому ученые стремились обнаружить его в отделе мозга, отвечающем за эти функции — в гиппокампе. Большое количество ацетилхолиновых нейронов направляет свои отростки в гиппокамп, и там они влияют на высвобождение нейромедиаторов из других нервных клеток [8]. Способ осуществления этого процесса довольно простой: на теле нейрона и его пресинаптической части расположены различные никотиновые рецепторы (в основном, α7— и β2-типов). Их активация будет приводить к тому, что прохождение сигнала по иннервируемой клетке упростится, и он с большей вероятностью перейдет на следующий нейрон. Наибольшее влияние такого рода испытывают на себе ГАМК-ергические нейроны — нервные клетки, чьим нейромедиатором является γ-аминомасляная кислота [9].
ГАМК-ергические нейроны являются важной частью системы, генерирующей электрические ритмы нашего мозга. Эти ритмы можно записать и изучить при помощи электроэнцефалограммы — широкодоступного метода исследования в нейрофизиологии. Ритмы различной частоты обозначаются греческими буквами: 8–14 Гц — альфа-ритм, 14–30 Гц — бета-ритм и так далее. Использование стимуляторов ацетилхолиновых рецепторов приводит к тому, что в мозге возникает тета- (0,4–14 Гц) и гамма-ритм (30–80 Гц). Эти ритмы, как правило, сопровождают активную когнитивную деятельность. Стимуляция постсинаптических мускариновых ацетилхолиновых рецепторов, расположенных на нейронах гиппокампа (центра памяти) и префронтальной коры (центр сложных форм поведения), приводит к возбуждению этих клеток и генерации упомянутых выше ритмов. Они сопровождают различную когнитивную деятельность — например, выстраивание временнόй последовательности событий [10].
Гиппокамп и префронтальная кора играют важную роль в обучении. С точки зрения рефлексов любое обучение происходит двумя путями. Допустим, вы экспериментатор, и объектом вашего эксперимента является мышь. В первом случае в ее клетке зажигается свет (условный стимул), и грызун получает кусочек сыра (безусловный стимул) еще до того, как свет погаснет. Формирующийся рефлекс можно назвать задержанным. Во втором случае свет также зажигается, но мышь получает лакомство через некоторое время после выключения лампочки. Этот тип рефлекса называется следовым. Рефлексы второго типа зависят от осознанности стимулов больше, чем рефлексы первого типа. Угнетение активности ацетилхолинергической системы приводит к тому, что у животных не вырабатываются следовые рефлексы, хотя с задержанными проблем не возникает [11].
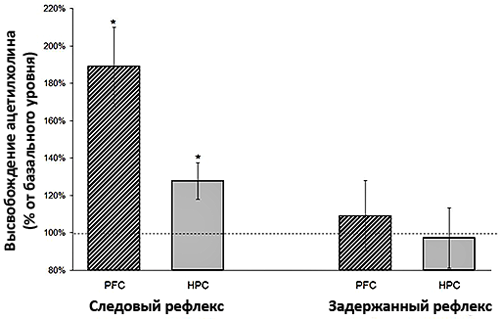
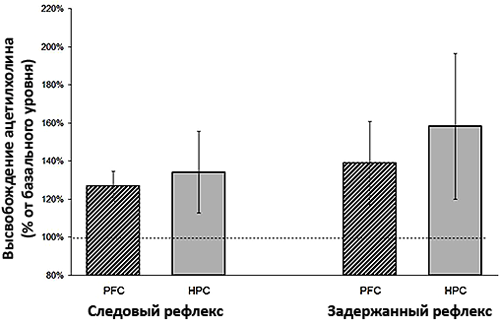
При сравнении секреции ацетилхолина в мозге крыс, у которых вырабатывали оба вида рефлексов, были получены интересные данные [12]. У крыс, которые успешно справлялись с усвоением временнόй связи между условным и безусловным стимулом, обнаруживалось значительное увеличение уровня ацетилхолина в медиальной префронтальной коре (рис. 5) по сравнению с гиппокампом. Особенно существенной была разница в уровнях ацетилхолина у крыс, которые выработали следовый рефлекс. Те грызуны, которые не справились с обеими задачами, обнаруживали приблизительно равные уровни нейромедиатора в исследуемых отделах мозга (рис. 6). Исходя из этого можно заключить, что непосредственно в обучении бóльшую роль играет префронтальная кора, а гиппокамп сохраняет полученные знания.
Рисунок 5. Выброс ацетилхолина в гиппокампе (HPC) и префронтальной коре (PFC) крыс при успешной выработке рефлексов. Максимальный уровень ацетилхолина наблюдается в префронтальной коре при выработке следового рефлекса. Рисунок из [12].
Рисунок 6. Выброс ацетилхолина в гиппокампе (HPC) и префронтальной коре (PFC) крыс в случае «провала» в обучении. Регистрируется почти одинаковое содержание ацетилхолина в двух зонах вне зависимости от рефлекса. Рисунок из [12].
Рецепторы внимания
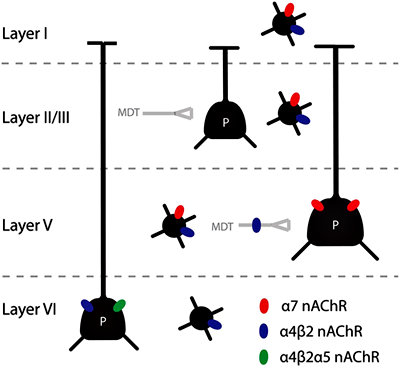
Рисунок 7. Многообразие ацетилхолиновых рецепторов (nAChR) в слоях префронтальной коры головного мозга. Рисунок из [15].
Для обучения важен не только интеллект или объем памяти, но и внимание. Без внимания даже самый успешный ученик будет двоечником. Ацетилхолин участвует также в процессах, регулирующих внимание.
Внимание — сфокусированное восприятие или обдумывание проблемы — сопровождается повышенной активностью в префронтальной коре. Ацетилхолиновые волокна направляются в лобную кору из глубоких отделов мозга. В связи с тем, что часто нам требуется быстрое переключение внимания, вполне логично, что в регуляции внимания участвуют никотиновые (ионотропные) рецепторы ацетилхолина, а не мускариновые, которые вызывают более медленные и преимущественно структурные изменения в нейронах. Повреждение ацетилхолиновых структур глубоких отделов мозга снижает активность медиальной префронтальной коры и нарушает внимание [13]. Кроме того, взаимодействие глубоких ацетилхолиновых структур с префронтальной корой не ограничивается восходящими сигналами. Нейроны лобной коры также отправляют свои сигналы в нижележащие отделы, что позволяет создавать саморегулирующуюся систему поддержания внимания [14]. Внимание поддерживается за счет воздействия ацетилхолина на пресинаптические и постсинаптические рецепторы (рис. 7).
При разговоре о никотиновых рецепторах и внимании возникает вопрос об улучшении когнитивных функций при помощи курения, то есть введения дополнительной дозы никотина, пусть и в виде сигаретного дыма [16]. Ситуация здесь довольно ясная, и результаты не дают курильщикам лишнего аргумента в пользу их пагубного пристрастия. Никотин, пришедший извне, нарушает нормальное развитие мозга, что может приводить к расстройствам внимания (на долгие годы) [17]. Если сравнивать курильщиков и некурящих, то у первых показатели внимания хуже, чем у их оппонентов [18]. Улучшение внимания у курильщиков возникает в случае выкуривания сигареты после долгого воздержания, когда их плохое настроение и когнитивные проблемы улетучиваются вместе с дымом.
Лекарство для памяти
Если в норме ацетилхолинергическая система нашего мозга отвечает за память, внимание и обучение, то заболевания, при которых нарушается этот тип трансмиссии в нашем мозге, должны проявляться соответствующими симптомами: потерей памяти, снижением внимания и способности учиться новому. Здесь надо сразу оговориться, что в ходе нормального старения у подавляющего большинства людей снижается и способность к запоминанию нового, и живость ума в целом. Если эти нарушения выражены настолько, что мешают пожилому человеку заниматься повседневной деятельностью и удовлетворять свои повседневные потребности (обслуживать себя), то тогда врачи могут заподозрить деменцию. Если вы хотите узнать о деменции больше, то рекомендую начать с изучения информационного бюллетеня ВОЗ, посвященного этой патологии [19].
Строго говоря, деменция — это не отдельное заболевание, а синдром, встречающийся при ряде заболеваний. Одной из самых частых болезней, которая приводит к деменции, является болезнь Альцгеймера. Считается, что при болезни Альцгеймера в нервных клетках накапливается патологический белок β-амилоид [20, 21], который и нарушает деятельность нервных клеток, что в итоге приводит к их гибели. Кроме этой теории существует ряд других, которые имеют свои доказательства. Вполне вероятно, что при болезни Альцгеймера в клетках головного мозга разных пациентов происходят неодинаковые процессы, но приводят они к схожим симптомам. Однако β-амилоид интересен тем, что он может подавлять эффект, производимый ацетилхолином на клетку через никотиновые рецепторы [22]. Если у нас получится интенсифицировать ацетилхолинергическую передачу, то мы можем уменьшить проявления болезни и продлить самостоятельную жизнь человеку с деменцией.
К препаратам, используемым при деменции, относятся ингибиторы ацетилхолинэстеразы (АХЭ) — фермента, разрушающего ацетилхолин в синаптической щели. Применение ингибиторов АХЭ приводит к повышению содержания ацетилхолина в межнейронном пространстве и улучшению передачи сигнала. Исследование эффективности ингибиторов АХЭ при болезни Альцгеймера определило, что они способны уменьшить симптомы заболевания [23] и замедлить его прогрессирование [24]. Три наиболее применяемых препарата из этой группы — ривастигмин, галантамин и донепезил — сравнимы по эффективности и безопасности. Также существует небольшой, но успешный опыт применения ингибиторов АХЭ в лечении музыкальных галлюцинаций у пожилых людей [25].
При помощи ацетилхолина наш мозг обучается, фокусирует внимание на разных объектах и явлениях окружающего мира. Наша память «работает» на ацетилхолине, а его дефицит можно компенсировать при помощи лекарств. Надеюсь, что вам понравилось знакомство с ацетилхолином.