Обструктивное апноэ во сне реферат
Что такое апноэ во сне? Причины возникновения, диагностику и методы лечения разберем в статье доктора Бормина С. О., сомнолога со стажем в 7 лет.
Определение болезни. Причины заболевания
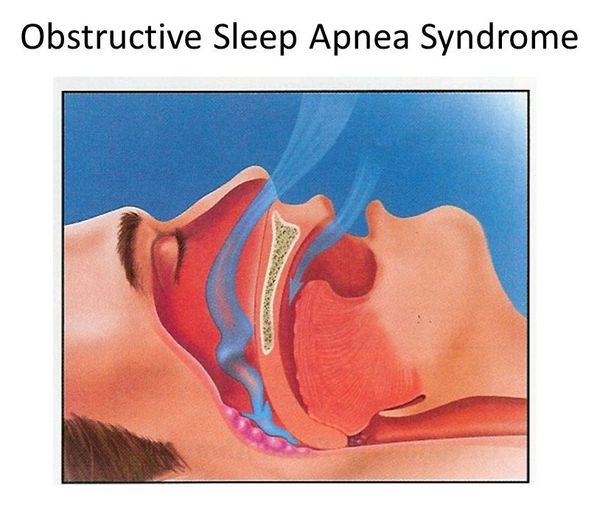
Апноэ сна — приостановка дыхания в процессе сна, которое приводит к полному отсутствию или уменьшению лёгочной вентиляции (более 90% по отношению к исходному воздушному потоку) продолжительностью от 10 секунд. Нарушение дыхания бывает двух видов: обструктивное и центральное. Их существенное различие заключается в дыхательных движениях: они имеют место при обструктивном типе и отсутствуют при центральном. Последний тип апноэ является редким случаем заболевания. Поэтому более детальному рассмотрению подлежит обструктивное апноэ сна как часто встречающаяся разновидность апноэ.
Синдром обструктивного апноэ сна (далее СОАС) — состояние, которому характерены:
Распространённость этого заболевания велика и составляет, по разным источникам, от 9 до 22% среди взрослого населения. [1]
Причина возникновения данного заболевания, как следует из названия, — обструкция дыхательных путей. К ней приводят различные патологии ЛОР-органов (чаще гипертрофия миндалин, у детей — аденоиды), а также снижение тонуса мышц, в том числе из-за увеличения массы (жировая ткань откладывается в стенках воздухоносных путей, сужая просвет и понижая тонус гладкой мускулатуры).
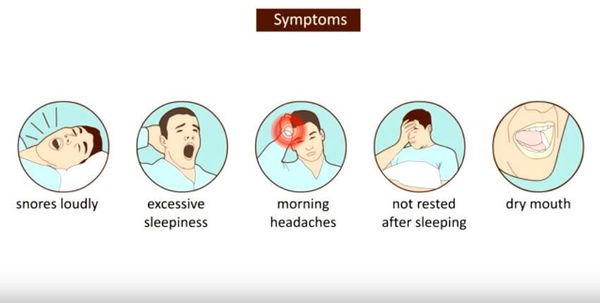
Симптомы апноэ во сне
Одним из самых частых и обращающих на себя внимание симптомов является храп. Распространённость его во взрослом населении составляет 14–84%. [2] Многие думают, что храпящие люди не страдают СОАС, поэтому храп не опасен для здоровья и является лишь раздражителем для второй половинки и социальным фактором. Однако, это не совсем так. У большинства пациентов с храпом имеются нарушения дыхания разной степени тяжести, и такой звуковой феномен может выступать в качестве самостоятельного патологического фактора за счёт вибрационной травмы мягких тканей глотки. [3] Чаще всего симптомы СОАС отмечают близкие, с ужасом фиксирующие резкое прекращение храпа и остановку дыхания, при этом человек совершает попытки вздохнуть, а после он начинает громко храпеть, иногда ворочается, двигает руками или ногами, и через время вновь восстанавливается дыхание. При тяжёлой степени больной может не дышать половину времени сна, а иногда и больше. Апноэ могут фиксироваться также и самим пациентом. При этом человек может просыпаться от ощущения нехватки воздуха, удушья. Но чаще всего пробуждение не наступает, и человек продолжает спать с прерывистым дыханием. В случаях, если человек спит в помещении один, данный симптом очень долгое время может оставаться незамеченным. Впрочем, как и храп.
К другим, не менее серьезным симптомам данного заболевания относятся:
Зачастую такие симптомы, как дневная сонливость и неосвежающий сон, пациенты недооценивают, считая, что они абсолютно здоровы. [4] Во многом это осложняет диагностику и приводит к ложной интерпретации симптомов. Также многие люди связывают учащённое ночное мочеиспускание с урологическими проблемами (цистит, аденома простаты и др.), многократно обследуются у врачей-урологов и не находят никакой патологии. И это правильно, потому что при выраженных нарушениях дыхания во сне частое ночное мочеиспускание является прямым следствием патологического процесса за счёт воздействия на выработку натрий-уретического пептида. [5]
Патогенез апноэ во сне
Возникающее спадение дыхательных путей приводит к прекращению поступления воздуха в лёгкие. Вследствие этого концентрация кислорода в крови падает, что приводит к короткой активации головного мозга (микропробуждения, повторяющиеся многократно, их пациент не помнит утром). После этого кратковременно нарастает тонус мышц глотки, расширяется просвет, и происходит вдох, сопровождающийся вибрацией (храпом). Постоянная вибрационная травма стенок глотки провоцирует дальнейшее падение тонуса. Вот почему нельзя рассматривать храп как безобидный симптом.
Постоянное снижение кислорода приводит к определённым гормональным перестройкам, которые изменяют углеводный и жировой обмен. При тяжёлых изменениях постепенно может возникнуть сахарный диабет 2 типа и ожирение, причём снизить вес, не устраняя основную причину, зачастую невозможно, однако нормализация дыхания может привести к значимому снижению веса без жёстких диет и изнуряющих упражнений. [6] Неоднократно повторяющиеся микропробуждения не дают пациенту погрузиться в стадию глубокого сна, тем самым вызывая дневную сонливость, утренние головные боли, стойкое повышению АД, особенно в предутренние часы и сразу после пробуждения.
Классификация и стадии развития апноэ во сне
Синдром обструктивного апноэ сна имеет три степени тяжести. [7] Критерием для деления служит индекс апноэ-гипопноэ (далее ИАГ) — количество дыхательных остановок за период одного часа сна (для полисомнографии) или в час исследования (для респираторной полиграфии). Чем больше этот показатель, тем тяжелее заболевание.
МКБ-10
Общие сведения
Синдром сонных (ночных) апноэ – расстройство дыхательной функции, характеризующееся периодическими остановками дыхания во сне. Кроме ночных остановок дыхания для синдрома сонных апноэ характерны постоянный сильный храп и выраженная дневная сонливость. Остановка дыхания во сне является потенциально опасным для жизни состоянием, сопровождающимся гемодинамическими расстройствами и нестабильной сердечной деятельностью.
Дыхательные паузы продолжительностью 10 секунд при синдроме сонных апноэ вызывают гипоксию (недостаток кислорода) и гипоксемию (повышение углекислоты), стимулирующие головной мозг, что ведет к частым пробуждениям и возобновлению дыхания. После нового засыпания вновь следует кратковременная остановка дыхания и пробуждение. Количество эпизодов апноэ зависит от тяжести нарушений и может повторяться от 5 до 100 раз в час, складываясь в общую продолжительность дыхательных пауз до 3-4 часов за ночь. Развитие синдрома сонных апноэ нарушает нормальную физиологию сна, делая его прерывистым, поверхностным, некомфортным.
Причины
Нарушения регуляции дыхательной функции со стороны ЦНС при синдроме центральных сонных апноэ могут вызываться травмами, сдавлениями стволового отдела головного мозга и задней черепной ямки, поражениями головного мозга при синдроме Альцгейма-Пика, постэнцефалитическом паркинсонизме. У детей встречается первичная недостаточность дыхательного центра, вызывающая синдром альвеолярной гиповентиляции, при котором наблюдается цианотичность кожных покровов, эпизоды апноэ во сне при отсутствии легочной или кардиальной патологии.
Синдром обструктивных сонных апноэ чаще встречается у лиц, страдающих ожирением, эндокринными расстройствами, подверженных частым стрессам. К развитию обструктивного синдрома апноэ во сне предрасполагают анатомические особенности верхних дыхательных путей: короткая толстая шея, узкие носовые ходы, увеличенное мягкое небо, миндалины или небный язычок. В развитии синдрома сонных апноэ имеет значение наследственный фактор.
Патогенез
Классификация
По патогенетическому механизму развития синдрома сонных апноэ выделяют его центральную, обструктивную и смешанную формы. Синдром центральных сонных апноэ развивается в результате нарушения центральных механизмов регуляции дыхания вследствие органических поражений головного мозга или первичной недостаточности дыхательного центра. Апноэ во сне при центральной форме синдрома обусловлено прекращением поступления к дыхательной мускулатуре нервных импульсов. Этот же механизм развития лежит в основе периодического дыхания Чейн-Стокса, которое характеризуется чередованием поверхностных и редких дыхательных движений с частыми и глубокими, переходящими затем в апноэ.
Синдром обструктивных сонных апноэ развивается вследствие спадения или окклюзии верхних дыхательных путей при сохранении дыхательной регуляции со стороны ЦНС и активности дыхательной мускулатуры. Некоторые авторы включают синдром обструктивных сонных апноэ в синдромный комплекс обструктивных апноэ-гипноэ, к которому также относится ряд респираторных дисфункций, развивающихся во сне:
Синдром смешанных сонных апноэ включает комбинацию механизмов центральной и обструктивной формы. По количеству эпизодов апноэ устанавливается степень тяжести течения синдрома сонных апноэ:
Симптомы
Зачастую пациенты с синдромом сонных апноэ сами не подозревают о своем заболевании и узнают о нем от тех, кто спит рядом. Основными проявлениями синдрома сонных апноэ служат храп, беспокойный и прерывистый сон с частыми пробуждениями, эпизоды остановок дыхания во сне (по свидетельству лиц, окружающих пациента), чрезмерная двигательная активность во сне.
В результате неполноценного сна у пациентов развиваются нейрофизиологические нарушения, проявляющиеся головными болями по утрам, разбитостью, избыточной дневной сонливостью, снижением работоспособности, раздражительностью, утомляемостью в течение дня, снижением памяти и концентрации внимания.
Со временем у пациентов, страдающих синдромом сонных апноэ, увеличивается масса тела, развивается половая дисфункция. Синдром сонных апноэ отрицательно влияет на сердечную функцию, способствуя развитию аритмий, сердечной недостаточности, приступов стенокардии. У половины пациентов с синдромом сонных апноэ имеется сопутствующая патология (артериальная гипертония, ИБС, бронхиальная астма, хроническая обструктивная болезнь легких и др.), значительно утяжеляющая течение синдрома. Развитие апноэ во сне нередко встречается при синдроме Пиквикка – заболевании, сочетающем недостаточность правых отделов сердца, ожирение и дневную сонливость.
У детей о синдроме сонных апноэ могут свидетельствовать дыхание через рот в дневное время, ночное и дневное недержание мочи, чрезмерная потливость во сне, сонливость и медлительность, поведенческие нарушения, сон в необычных позах, храп.
Осложнения
Нарушения сна при синдроме сонных апноэ может тяжело отразиться на качестве жизни. Снижение концентрации внимания в дневное время повышает риск травматизма и несчастных случаев на производстве, в быту и повседневной деятельности.
Увеличение частоты эпизодов апноэ прямо влияет на повышение уровня утреннего артериального давления. Во время дыхательных пауз может развиваться нарушение сердечного ритма. Все чаще синдром сонных апноэ называют причиной развития инсульта у молодых мужчин, ишемии и инфаркта миокарда у пациентов с атеросклерозом. Синдром сонных апноэ утяжеляет течение и прогноз хронической легочной патологии: ХОБЛ, бронхиальной астмы, хронического обструктивного бронхита и т. д.
Диагностика
В распознавании синдрома сонных апноэ важен контакт с родственниками пациента и их участие в установлении факта остановок дыхания во сне. Для диагностики синдрома сонных апноэ в амбулаторной практике используется метод В. И. Ровинского: один из родственников во время сна пациента засекает с помощью часов с секундной стрелкой продолжительность дыхательных пауз.
При осмотре у пациентов обычно определяется индекс массы тела (ИМТ) > 35, что соответствует II степени ожирения, окружность шеи > 40 см у женщин и 43 см у мужчин, показатели артериального давления превышают 140/90 мм рт. ст.
Пациентам с синдромом сонных апноэ проводится консультация отоларинголога, в ходе которой нередко выявляется патология ЛОР-органов: ринит, синусит, искривление перегородки носа, хронический тонзиллит, полипоз и др. Исследование носоглотки дополняется фарингоскопией, ларингоскопией и риноскопией с помощью гибкого фиброэндоскопа.
Достоверную картину наличия синдрома сонных апноэ позволяет установит проведение полисомнографического исследования. Полисомнография сочетает в себе длительную (свыше 8 часов) одновременную регистрацию электрических потенциалов (ЭЭГ головного мозга, ЭКГ, электромиограммы, электроокулограммы) и респираторной активности (воздушных потоков, проходящих через рот и нос, дыхательных усилий мускулатуры брюшной и грудной полости, насыщение (SaO 2) крови кислородом, феномена храпа, позы тела во время сна). При анализе записи полисомнографии определяется количество и длительность эпизодов апноэ во сне и степень выраженности происходящих при этом изменений.
Вариантом полисомнографии является полиграфическое исследование – ночная регистрация электрических потенциалов организма, включающая от 2 до 8 позиций: ЭКГ, носового дыхательного потока, грудного и брюшного усилия, насыщения кислородом артериальной крови, мышечной активности нижних конечностей, звукового феномена храпа, позиции тела во время сна.
Лечение синдрома сонных апноэ
Программа лечения может включать использование немедикаментозных, медикаментозных и хирургических методов воздействия на причину заболевания. Общие рекомендации при нетяжелых нарушениях ночного дыхания включают сон с приподнятым головным концом кровати (на 20 см выше обычного), исключение сна в положении на спине, закапывание на ночь ксилометазолина (галазолина) в нос для улучшения носового дыхания, полоскание горла раствором эфирных масел, лечение патологии ЛОР-органов (хронического ринита, синусита), эндокринопатий, исключение приема снотворных и алкоголя, снижение веса.
Во время сна возможно применение различных оральных приспособлений (выдвигателей нижней челюсти, удерживателей языка), способствующих поддержанию просвета дыхательных путей, кислородотерапии.
Использование чрезмасочной аппаратной СИПАП–терапии (СИПАП-вентиляции), обеспечивающей поддержание постоянного положительного давления воздухоносных путей, позволяет нормализовать ночное дыхание и улучшить дневное самочувствие пациентов с синдромом сонных апноэ. Этот метод на сегодняшний день считается наиболее перспективным и эффективным. Назначение приема теофиллина не всегда дает желаемый эффект у пациентов с обструктивным ночным апноэ. При центральной форме синдрома сонных апноэ возможен положительный эффект от приема ацетазоламида.
Оперативные вмешательства при синдроме сонных апноэ рассматриваются как вспомогательные в случаях имеющихся аномалий и дефектов в строении верхних респираторных путей или их хронических заболеваниях. В ряде случает аденоидэктомия, коррекция носовой перегородки и тонзиллэктомия позволяют полностью устранить причины синдрома сонных апноэ. Операции по увулопалатофарингопластике и трахеостомии проводятся при крайне тяжелых расстройствах.
Прогноз и профилактика
Показатели уровня смертности у пациентов с синдромом сонных апноэ в 4,5 раза превышают таковые в общей популяции. Применение СРАР-терапии позволило сократить уровень смертности на 48% и увеличить продолжительность жизни на 15 лет. Однако, этот метод не оказывает воздействия на патогенез синдрома сонных апноэ.
Профилактика возможных осложнений апноэ во сне диктует необходимость участия в лечении синдрома специалистов пульмонологов, отоларингологов, кардиологов, неврологов. В случае синдрома сонных апноэ можно говорить только о проведении неспецифической профилактики, включающей в себя нормализацию веса, отказ от курения, приема снотворных препаратов, алкоголя, лечение заболеваний носоглотки.
Синдром обструктивного апноэ сна
Для понимания актуальности проблемы приведем клинический пример. Пациент К. 59 лет, поступил в отделение медицины сна Клинического санатория «Барвиха» 9 апреля 2009 г. с жалобами на повышение артериального давления преимущественно в утренние часы, храп, о
Для понимания актуальности проблемы приведем клинический пример. Пациент К. 59 лет, поступил в отделение медицины сна Клинического санатория «Барвиха» 9 апреля 2009 г. с жалобами на повышение артериального давления преимущественно в утренние часы, храп, остановки дыхания во сне с последующими всхрапываниями (со слов окружающих), пробуждения от нехватки воздуха и приступов удушья, изжогу по ночам, приступообразный ночной кашель, учащенное ночное мочеиспускание (3–5 раз за ночь полным мочевым пузырем), неосвежающий сон, разбитость и головную боль по утрам, резкую дневную сонливость.
Анамнез: храп отмечает около 10 лет, за это время вес увеличился на 10 кг. Прочие указанные выше жалобы появились около пяти лет назад и постепенно нарастали. Родственники постоянно обращали внимание на остановки дыхания во сне. По поводу вышеперечисленных жалоб пациент неоднократно обращался к врачам, но диагноза «апноэ сна» не выставлялось. За несколько дней до поступления в санаторий «Барвиха» пациент обратился к неврологу с жалобами на плохой сон. Пациенту был назначен Феназепам на ночь, на фоне приема которого у пациента в ранние утренние часы развился тяжелый гипертонический криз, и он был госпитализирован в кардиологическое отделение. На следующее утро сосед по палате рассказал пациенту, что тот громко храпел, периодически переставал дышать на минуту и более и при этом синел. И именно сосед предположил, что у пациента имеется апноэ сна, и порекомендовал обратиться в медицинский центр, где ему смогут помочь. Родственники пациента нашли информацию об отделении медицины сна санатория «Барвиха» в интернете.
При проведении полисомнографии (рис. 1) в отделении у пациента зарегистрировано 364 эпизода апноэ и 22 эпизода гипопноэ обструктивного генеза. Индекс апноэ + гипопноэ = 58 в час. Максимальная остановка дыхания составила 87 секунд. Эпизоды апноэ сопровождались резкими десатурациями (минимальная сатурация — 64%). Следует отметить, что при сатурации ниже 70% развивается диффузный цианоз. У пациента был выставлен диагноз: «синдром обструктивного апноэ сна, тяжелая форма».
В приведенной истории болезни обращает на себя внимание тот факт, что, несмотря на классическую клиническую картину заболевания, диагноз был поставлен не врачами, к которым пациент регулярно обращался, а соседом по палате. Таким образом, врачи еще недостаточно информированы о клинической значимости апноэ сна. А назначение Феназепама у пациента с апноэ сна можно расценить как грубую диагностическую и лечебную ошибку.
Итак, статья будет посвящена синдрому обструктивного апноэ сна (СОАС) — состоянию, характеризующемуся наличием храпа, периодическим спадением верхних дыхательных путей на уровне глотки и прекращением легочной вентиляции при сохраняющихся дыхательных усилиях, снижением уровня кислорода крови, грубой фрагментацией сна и избыточной дневной сонливостью [Guilleminault C., 1976].
Классификация, эпидемиология
Из определения СОАС видно, что в основе болезни лежит периодическое прекращение дыхания из-за спадения стенок дыхательных путей на уровне глотки во сне. Дыхательные пути могут спадаться полностью, и тогда развивается апноэ — прекращение воздушного потока (легочной вентиляции) длительностью 10 c и более. При неполном спадении дыхательных путей отмечается гипопноэ — существенное снижение воздушного потока (более 50% от исходных значений), сочетающееся со снижением насыщения гемоглобина артериальной крови кислородом (сатурации) на 3% и более.
Общепризнанным критерием степени тяжести СОАС является суммарная частота апноэ и гипопноэ в час — индекс апноэ/гипопноэ (ИАГ). Считается нецелесообразным подсчитывать отдельно количество апноэ и гипопноэ, так как они несут схожие риски в отношении развития сердечно-сосудистых и иных осложнений. В настоящее время большинство международных консенсусов и клинических рекомендаций придерживаются классификации, приведенной в табл.
Распространенность СОАС составляет 5–7% от всего населения старше 30 лет. Тяжелыми формами заболевания страдают около 1–2% из указанной группы лиц (Stradling J. R. и соавт., 1991). Данные показатели сопоставимы с распространенностью бронхиальной астмы (Young T. и соавт., 1993). У лиц старше 60 лет частота СОАС значительно возрастает и составляет около 30% у мужчин и около 20% у женщин. У лиц старше 65 лет частота заболевания может достигать 60% [Ancoli-Israel S., 1991]. Частота СОАС может достигать 50% и более у пациентов с рефрактерной к лечению артериальной гипертонией, ночными брадиаритмиями, ожирением 3–4 степени, метаболическим синдромом, пиквикским синдромом, гипотиреозом и рядом других заболеваний.
Этиология и патогенез
В основе патогенеза СОАС лежит периодическое спадение исходно суженных верхних дыхательных путей на уровне глотки во время сна. Причинами сужения могут быть:
Дополнительный вклад в проблему вносит снижение тонуса глоточных мышц, обусловленное рядом факторов:
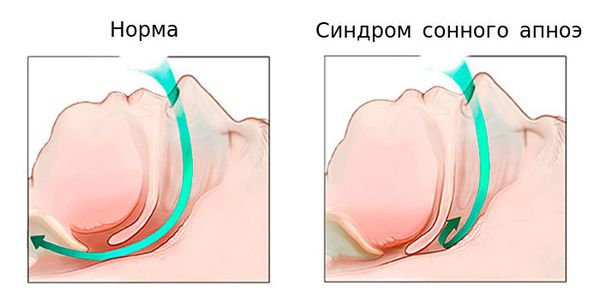
Зона, в которой наступает спадение, может находиться на уровне мягкого неба, корня языка или надгортанника, то есть в нижней части носоглотки и ротоглотке (рис. 2). Реализация указанного механизма обструкции дыхательных путей в патологическое состояние происходит следующим образом. Человек засыпает.
Происходит постепенное расслабление мышц глотки и увеличение подвижности ее стенок. Один из очередных вдохов приводит к полному спадению дыхательных путей и прекращению легочной вентиляции. При этом дыхательные усилия сохраняются и даже усиливаются в ответ на развивающуюся гипоксемию. Острый недостаток кислорода приводит к стрессовой реакции, сопровождающейся активацией симпатоадреналовой системы и подъемом АД. В конце концов, негативная информация от различных органов и систем доходит до мозга и вызывает его частичное пробуждение (активацию). Мозг, в свою очередь, восстанавливает контроль над глоточной мускулатурой и открывает дыхательные пути. Человек громко всхрапывает, делает несколько глубоких вдохов. В организме восстанавливается нормальное содержание кислорода, мозг успокаивается и засыпает вновь… Цикл повторяется снова. За ночь может отмечаться до 400–500 остановок дыхания по 20–30 секунд. Суммарная длительность апноэ может достигать 3–4 часов из 8 часов сна. Это в свою очередь существенно увеличивает риск развития артериальной гипертензии, нарушений ритма сердца, инфаркта миокарда, инсульта и внезапной смерти во сне.
Marin J. M. и соавт. (2005) провели 10-летнее наблюдение и получили достоверное 3 кратное увеличение фатальных (смерть от инфаркта миокарда или инсульта) осложнений и 4–5 кратное увеличение нефатальных сердечно-сосудистых событий (инфаркт, инсульт, операция коронарного шунтирования или баллонной ангиопластики) у пациентов с нелеченным тяжелым СОАС по сравнению со здоровыми добровольцами и пациентами с неосложненным храпом.
При тяжелых формах СОАС развиваются специфические гормональные расстройства. В частности, это касается снижения продукции соматотропного гормона (гормона роста) и тестостерона, пики секреции которых отмечаются в глубоких стадиях сна [Gronfier C. и соавт., 1996]. При СОАС глубокие стадии сна практически отсутствуют, что ведет к недостаточной продукции указанных гормонов [Grunstein R. R. и соавт., 1989]. Одной из функций соматотропного гормона у взрослых людей является регуляция жирового обмена и, в частности, мобилизация жира из депо. При недостатке соматотропина накопленный жир не может превратиться в энергию. Все образующиеся излишки ложатся «мертвым грузом», который не может быть востребован [Rudman D. и соавт., 1990]. Человек начинает полнеть, причем любые усилия, диетические или медикаментозные, направленные на похудание, оказываются малорезультативными. Более того, жировые отложения на уровне шеи приводят к дальнейшему сужению дыхательных путей и прогрессированию СОАС, а это в свою очередь усугубляет недостаток соматотропного гормона. Таким образом, создается порочный круг, разорвать который без специального лечения СОАС практически невозможно [Grunstein R. R. и соавт., 1989]. Недостаток тестостерона в организме ведет к снижению либидо и импотенции у мужчин.
Клиническая картина
В клинической картине, прежде всего, обращает на себя внимание типичный портрет пациента, страдающего СОАС. Обычно это полный человек с гиперстенической конституцией, красным или багрово-синюшным одутловатым лицом, инъецированными сосудами склер и хриплым голосом. Характерный вид пациента с СОАС был описан еще Чарльзом Диккенсом в «Посмертных записках Пиквикского клуба». Это был толстяк с короткой шеей и красным лицом, который постоянно засыпал и начинал храпеть в самых неудобных ситуациях.
Для выявления остановок дыхания во сне проще всего понаблюдать за спящим человеком. Обычно сразу после засыпания у человека появляется храп. Вскоре у больного внезапно останавливается дыхание. В это время не слышно дыхательных шумов, храп прекращается. Однако больной пытается дышать, что видно по движениям грудной клетки и брюшной стенки. Примерно через 15–30 секунд человек громко всхрапывает и делает несколько глубоких вдохов и выдохов. Как правило, сон больного очень беспокоен: он вертится в постели, двигает руками и ногами, иногда что-то говорит.
При СОАС могут отмечаться следующие симптомы:
Диагностика
Для скрининга нарушений дыхания во сне может применяться компьютерная мониторинговая пульсоксиметрия — метод длительного мониторирования сатурации и пульса. Компьютерный пульсоксиметр выполняет до 30 000 измерений сатурации и пульса за 8 часов сна и сохраняет полученные данные в памяти. Дальнейшая компьютерная обработка данных позволяет с высокой точностью оценивать средние параметры сатурации, проводить визуальный анализ оксиметрических трендов, выявлять острые эпизоды падения насыщения крови кислородом, характерные для апноэ. Количественная оценка частоты десатураций в час (индекс десатураций) позволяет косвенно судить о частоте эпизодов апноэ/гипопноэ в час (ИАГ).
Для точной диагностики храпа и болезни остановок дыхания во сне используется полисомнография — метод длительной регистрации различных функций человеческого организма в период сна (рис. 1). Исследование позволяет поставить точный диагноз, оценить сердечно-сосудистые и неврологические риски и определить оптимальную тактику лечения.
Одним из многообещающих направлений диагностики расстройств дыхания во сне является добавление к классическим холтеровским мониторам каналов регистрации пневмограммы, сатурации и потока воздуха. Данные системы уже имеются на отечественном рынке. Фактически выполняется полифункциональное холтеровское мониторирование ЭКГ и параметров дыхания во время сна, которое позволяет поставить собственно диагноз СОАС, а также оценить связь ночной ишемии миокарда, аритмий и блокад с нарушениями ритма во сне. Методика имеет большие перспективы как в специализированных аритмологических центрах, так и в учреждениях практического здравоохранения, занимающихся холтеровским мониторированием.
Лечение
Объем статьи позволяет нам лишь в общих чертах описать подходы к лечению храпа и СОАС. Следует подчеркнуть, что выбор конкретного метода или совокупности методов лечения у конкретного пациента зависит от сочетания причин и тяжести расстройств дыхания во сне.
Прежде всего, следует отметить, чего категорически нельзя делать у пациентов с СОАС — это назначать снотворные и транквилизаторы, обладающие миорелаксирующим и респираторно-депрессивным действием, например, бензодиазепиновые транквилизаторы [Вейн А. М., 2002]. В начале статьи мы упоминали пациента, которому был назначен Феназепам, который, по всей видимости, существенно ухудшил состояние и вызвал гипертонический криз. На уровне первичного звена здравоохранения, когда дефицит времени и ресурсов не позволяет исключить СОАС у пациентов с жалобами на плохой сон, а клиническая ситуация требует назначения снотворных, можно с осторожностью, взвешивая пользу и риски, назначать гипнотики, которые в наименьшей степени влияют на респираторную функцию. К ним относятся Донормил или небензодиазепиновые агонисты бензодиазепиновых рецепторв (Z-группа), например, Санвал.
Общепрофилактические мероприятия у пациентов с храпом и СОАС включают снижение массы тела, прекращение курения, ограничение потребления алкоголя, сон на боку. При неосложненном храпе возможно использование спреев для горла, облегчающих храп.
У пациентов с ретро- и микрогнатией возможно применение внутриротовых аппликаторов, смещающих вперед нижнюю челюсть.
При наличии явных анатомических препятствий на уровне носа и глотки (искривление носовой перегородки, резкая гипертрофия миндалин) требуется соответствующее хирургическое лечение.
Следует отдельно остановиться на селективных оперативных вмешательствах на мягком небе (лазерных или радиочастотных). При неосложненном храпе у пациентов с достаточно широким просветом глотки и исходно удлиненным небным язычком эти вмешательства эффективны. Однако у пациентов с исходно узкой глоткой и среднетяжелыми формами СОАС наблюдается мультисегментарное спадение дыхательных путей на уровне неба, корня языка и даже надгортанника. В этой ситуации подрезание небного язычка практически не дает эффекта в отношении апноэ сна. Более того, если после лазерного или радиочастотного ожога происходит ретракция тканей глотки, это может еще больше ее сузить и привести к развитию фарингостеноза. В свете изложенного становится понятным, почему в Стандартах Американской академии медицины сна по применению лазерной увулопалатопластики для лечения храпа и апноэ сна (1994, пересмотр 2000 г.) первый же пункт гласит: «Лазерная увулопалатопластика не рекомендуется для лечения расстройств дыхания во сне, включая синдром обструктивного апноэ сна».
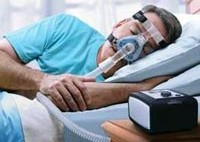
Основным методом лечения пациентов со среднетяжелой формой СОАС и ожирением является неинвазивная вспомогательная вентиляция легких постоянным положительным давлением во время ночного сна (СРАР-терапия — аббревиатура английских слов Continuous Positive Airway Pressure). Суть метода очень проста. Если дыхательные пути немного «раздувать» во время сна, то это будет препятствовать их спадению и устранит основной механизм развития заболевания. Лечение проводится с помощью небольшого компрессора, который подает в дыхательные пути постоянный поток воздуха через гибкую трубку и носовую маску.
Полный эффект лечения достигается в первую же ночь лечения. У больного исчезают храп, остановки дыхания и нормализуется ночной сон. В тяжелых случаях аппарат необходимо использовать каждую ночь. При более легком течении заболевания возможно периодическое применение аппарата (4–5 раз в неделю). Лечение практически не дает побочных эффектов. Отмена аппаратного лечения (даже если оно проводилось несколько лет) не влечет за собой каких-либо осложнений, за исключением постепенного возвращения исходной симптоматики. Применение аппарата не излечивает человека, но обеспечивает нормальный сон, улучшение качества жизни и профилактику серьезных осложнений.
В заключение следует отметить, что синдром обструктивного апноэ сна является актуальной проблемой современной медицины из-за большой распространенности этой патологии в популяции, увеличения риска сердечно-сосудистых осложнений и значительного ухудшения качества жизни пациентов. В настоящее время врач, информированный о данной проблеме, располагает возможностью своевременного выявления больных с этой потенциально летальной патологией. Вовремя назначенное лечение позволяет в подавляющем большинстве случаев предотвратить нежелательные последствия и значительно улучшить качество жизни пациента.
Литература
ФГУ «Клинический санаторий «Барвиха» Управления делами Президента РФ, Москва

.gif)