Репешок от псориаза рецепт
Клинический случай нефропатии обусловленной приемом репешка обыкновенного (agrimonia eupatoria)
1 Кафедра внутренних болезней с основами физиотерапии №2, Нефрологическое отделение ГБОУ ВПО РостГМУ Минздрава России, г.Ростов-на-Дону
2 Ростовское областное патологоанатомическое бюро Министерства здравоохранения Ростовской области, г.Ростов-на-Дону
Адрес: 344022, г. Ростов-на-Дону, пер. Нахичеванский, 29, тел. (863)2014423 Эл.почта: batjushin-m@rambler.ru, sadovnichaya@list.ru, nephr-roon@rambler.ru
За прошедшее десятилетие отмечен значительный рост популярности «нетрадиционной медицины». Это объясняется такими факторами, как неудовлетворенность методами и эффективностью ранее проводимого лечения, бесконтрольным использованием информации о неблагоприятных побочных действиях фармацевтических препаратов, ростом цен на фармакопейные лекарственные средства и низким уровнем общей культуры населения. В отношении использования сбора лекарственных растений в литературе имеются указания на ограничения их применения, так как их прием при определенных заболеваниях может вызывать нежелательные побочные эффекты. В Европе, США и Канаде постоянно увеличивается доля населения, регулярно использующего фитотерапевтические средства и биологически активные добавки, в странах Азии и Африки более 30% всех случаев острого почечного повреждения развивается как осложнение лечения растительными препаратами [1, 2]. По данным исследования импортированных патентованных азиатских аюрведических растительных продуктов в Калифорнии, было установлено, что 32% из них содержали не декларированные фармацевтические средства и тяжелые металлы (свинец, ртуть, кадмий, мышьяк). Среди не декларированных веществ наиболее часто встречаются: эфедрин, хлорфениламин, колхицин, метилтестостерон, глюкокортикостероиды, нестероидные противовоспалительные препараты [3, 4, 5, 6, 7, 8]. Сегодня в Европе зарегистрировано более 100 препаратов, содержащих растительные флавоноиды. Они обладают антиоксидантной активностью и применяются в основном в лечении нарушений периферического кровообращения.
Потенциальное значение этой проблемы чрезвычайно велико, в частности остается неясной степень взаимодействия фармацевтического препарата с травами и растительными продуктами [9, 10]. Неконтролируемый прием лекарственных трав может превышать потенциальный положительный эффект, особенно среди лиц с заболеваниями почек [11, 12, 13, 14], что связано с непосредственным воздействием растительных препаратов на клетки канальцев и их активной реабсорбцией с достижением высокой концентрации в мозговом слое. Результатом такого воздействия на почки является острое канальцевое повреждение, папиллярный некроз, острый и хронический интерстициальный нефрит, синдром Фанкони, нефролитиаз, артериальная гипертензия, рабдомиолиз [15, 16].
К фитотоксинам, обладающим прямым нефротропным действием относят аристохолиевую кислоту, сапонины, метилсалицилат, флавоноиды, ореллаин, алкалоиды эфедры, охратоксин [17]. На территории России наиболее часто с целью лечения и профилактики заболеваний почек применяются такие лекарственные травы как: пижма, барбарис, берѐза, бессмертник песчаный, брусника, бузина, календула, кукуруза (рыльца), можжевельник, толокнянка, хвощ, шиповник, репешок обыкновенный (Argimonia Eupatoria), а также марена красильная грузинская (Rubia tinctorum var. iberica), дикорастущая трава.
Репешок обыкновенный (Argimonia Eupatoria) – многолетнее травянистое растение, широко распространенное в европейской части России, на территории Западной и Восточной Сибири, Дальнего Востока [18]. В народной и традиционной медицине все части растения применяются при широком спектре заболеваний в качестве желчегонного, противовоспалительного, антиаритмического, гипогликемического, антигельминтного, анальгетического, гемостатического, антигипертонического, антитоксического и антиканцерогенного средства. В европейских странах некоторые виды Agrimonia являются официальными лекарственными растениями и используются в практической медицине как вяжущее, противовоспалительное средство [19]. При проведении биохимического анализа структуры растения в надземной части A.Eupatoria обнаружены вещества фенольной природы (филавоноиды, дубильные вещества, кумарины, изокумарины, оксикоричные кислоты), тритерпеноиды, эфирное масло, полисахариды и др., а в подземных органах растения обнаружены медь, цинк, железо, ванадий, никель, хром, титан, марганец, стронций, цирконий, серебро [20].
Токсические эффекты А. Eupatoria в большей степени связаны не со специфическими токсикантами, а с наличием в нем большого количества гликозидов кумарина и его метаболитами. В 1994 г. на основании углубленного анализа токсикологических исследований экспертами Европейского Совета сделаны рекомендации о снижении допустимого уровня содержания кумарина в продуктах питания до 0,5 мг/кг вследствие его канцерогенного и мутагенного действия.
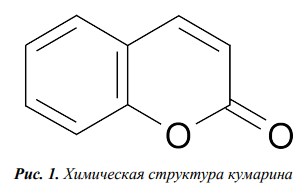
КУМАРИН (2-хроменон) имеет молекулярную массу 146,14 и представляет собой бесцветные кристаллы с запахом свежего сена и горьким вкусом (рисунок 1).
Рис. 1. Химическая структура кумарина
Сообщения о гепатотоксических эффектах для человека, развивающихся вследствие приема кумарин-содержащих лекарственных препаратов, часто противоречивые, вызвали значительный интерес исследователей к изучению его метаболизма и механизма токсического действия [20, 21].
Современные представления о метаболизме кумарина предполагают наличие двух основных путей трансформации данного соединения в организме млекопитающих. Первый этап трансформации кумарина реализуется по двум направлениям: в результате 7-гидроксилирования кумарина образуется малотоксичный 7-гидроксикумарин, элиминирующийся из организма млекопитающих с мочой; в процессе 3-гидроксилирования образуется 3-гидроксикумарин, промежуточным метаболитом в данном процессе является токсичный 3,4-эпоксид, подвергающийся дальнейшей трансформации с образованием о-гидроксифенилальдегида, окисляющегося до о-гидроксиэтанола и о-гидроксифенилуксусной кислоты. Рядом авторов было показано, что доминирование одного из двух направлений метаболизма кумарина в организме обусловливает межвидовые различия в проявлении гепатотоксических свойств данного соединения [22, 23]. Риск осложнений при приеме кумарина возрастает при сочетанном приеме НПВС, антикоагулянтов прямого и непрямого действия.
В экспериментальных работах [24, 25] установлено, что кумарин при однократном введении в больших дозах крысам вызывает центрилобуллярный некроз гепатоцитов. Это свидетельствует о том, что метаболизм кумарина [3-l4C] в данном случае проходил с образованием более токсичных метаболитов. Исследования in vitro показали, что химически активные [3-l4C]-кумариновые метаболиты, образующиеся при участии цитохром P450-зависимых энзимов, способны ковалентно связывать микросомальные протеины [26]. Было сделано предположение, что токсическим метаболитом в данном случае может выступать 3,4-эпоксид.
Нами представлен случай нефротоксического действия алкалоидов кумарина и его метаболитов при употреблении отваров и настоев Репешка обыкновенного.
Пациентка А. 43 лет, поступила в нефрологическое отделение клиники РостГМУ с жалобами на легкую ноющую боль в поясничной области с обеих сторон, усиливающуюся при физической нагрузке, пастозность голеней и стоп, периодически повышающееся артериальное давление до 220/140 мм рт. ст., не связанное с психоэмоциональными и/или физическими нагрузками, сопровождающееся головной болью и головокружением. Из анамнеза известно, что в 1990 году в течение всего периода первой беременности выявлялась протеинурия до 3,3 г/л, не сопровождающаяся отечным синдромом и артериальной гипертензией, в течение 5 лет после родов протеинурия сохранялась на уровне 0,5-1,0 г/л. В 1995 г. впервые зарегистрирован высокий уровень артериального давления (АД) – 150/100 мм рт. ст. Антигипертензивную терапию не получала, однако с 1999 г. артериальная гипертензия приобрела злокачественный характер, с повышением уровня системного АД до 200/120 мм рт. ст., по поводу чего в 2000 году проходила обследование в стационаре, где был поставлен диагноз гипертонической болезни II стадии, 3 степени, риск 3 (высокий), тогда же была подобрана антигипертензивная терапия, позволявшая контролировать АД на уровне 130-150/80-90 мм рт. ст., но пациентка данные рекомендации не соблюдала, а самостоятельно приобрела фитопрепарат (Репешок обыкновенный), отвар и настои которого, принимала более полугода непрерывно по несколько раз в сутки. В 2001 году, во время прохождения планового медицинского осмотра выявлен нефросклероз справа, дальнейшего наблюдения и лечения не проходила. В 2008 году при выполнении ультразвукового исследования почек выявлен конкремент правой сморщенной почки, по данным реносцинтиграфии функция правой почки отсутствует.
Помимо приема фитопрепаратов постоянно использует дипиридамол в дозе 75 мг/сутки, эналаприл 10 мг/сутки с 2001 года, в 2011 году уровень протеинурии составил 0,044 г/л, уровень артериального давления до 240/140 мм ртутного столба.
По данным клинико-лабораторного обследования в нефрологическом отделении клиники РостГМУ со стороны ОАК на себя обращали внимание ускорение СОЭ до 32 мм/час, признаки анемии легкой степени тяжести (эритроцитов 2,52х1012/л, гемоглобин 100 г/л), снижение количества тромбоцитов (75х103 /л), со стороны свертывающей системы крови по данным коагулограммы выявлены признаки гипокогуляции, характеризующиеся снижением АПТВ до 20 сек., протромбиновое время 10 сек., МНО 0,5, тромбиновое время 6 сек., фибриноген 1,98 г/л, со стороны биохимических показателей крови отмечалась гиперхолестеринемия до 10,79 мМ/л, гиперазотемия (креатинин крови 129 мкМ/л, мочевина 14,9 мМ/л), уровень АСТ достигал 68 Ед/л, АЛТ – 51 Ед/л. В ОАМ – протеинурия, характерная для нефритического синдрома (до 0,4 г/л). Снижение концентрационной функции почек, проявляющееся снижением СКФ до 45,5 мл/мин (по формуле MDRD), изостенурией (по данным пробы Фольгарда). Суточная протеинурия не превышала 0,495 г/сутки, по данным суточной экскреции солей с мочой отмечается высокая экскреция кальция до 9,73 мМ/сутки, и мочевой кислоты до 9,13 мМ/сутки. За все время наблюдения состояние пациентки оставалось стабильным, уровень АД в пределах 130-140/70-80 мм рт. ст., суточный диурез около 1500-1700 мл. По данным УЗИ почек отмечаются диффузные изменения паренхимы почек, уменьшение размеров, микролит правой почки.
Таким образом, клиническая картина болезни соответствовала аутоиммунному заболеванию почек, на что указывали наличие протеинурии, мочевой синдром, характеризующийся микрогематурией, снижением азотвыделительной функции почек, наличием артериальной гипертензии, тем не менее, нельзя было исключить наличие хронического повреждения канальцевого эпителия, преимущественно в проксимальных отделах, с нарушением реабсорбции, без формирования клиники острого канальцевого некроза, что позволило заподозрить наличие специфического патологического процесса, связанного с токсическим влиянием метаболита кумарина на канальцевый эпителий почек. Следует также учесть наличие процесса нефросклероза в правой почке, вероятно, обусловленного мочекаменной болезнью в анамнезе.
Пациентке была выполнена пункционная нефробиопсия левой почки с последующим морфологическим исследованием биоптата с целью верификации патологического процесса и определения тактики терапии. В результате получены следующие данные.
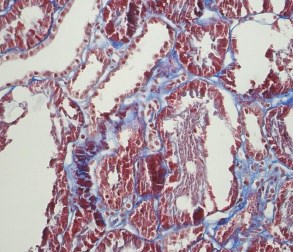
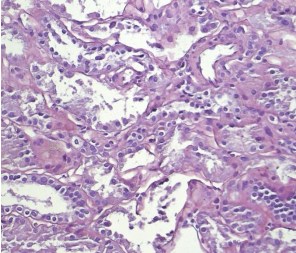
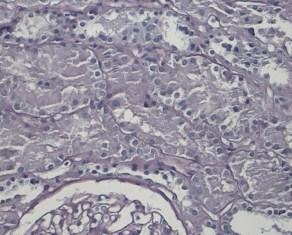
Светооптически 1 из 9 клубочков склерозирован полностью, остальные гипертрофированы. В одном клубочке выраженная интракапиллярная гиперклеточность и пролиферация базальных мембран. Остальные клубочки не имеют признаков выраженных пролиферативных изменений, за исключением сегментарного расширения парамезангиальных зон. Сегментарного склероза капиллярных пучков не наблюдается. В интерстиции слабый диффузный и мелкоочаговый фиброз. Резко выраженная гидропическая дистрофия эпителия канальцев вплоть до вакуолизации (рисунки 2, 3, 4).
Рис. 2. Х20 массон1 – резко выраженные дистрофические изменения эпителия канальцев, его слущивание
Рис. 3. Х20 ШИК – резко выраженные повреждения эпителия канальцев – слущивание фрагментов цитоплазмы и целых клеток в просвет канальцев
Рис. 4. Х20 ШИК – расширение и гиперклеточность мезангиальных зон
Окраска на амилоид отрицательна. Иммуноморфологически: IgA в клубочках: отрицательно, в канальцах: отрицательно, IgG в клубочках: отрицательно, в канальцах: отрицательно, IgM в клубочках: единичное редкое пунктирное, в канальцах: единичные цилиндры, C3 комплимент: единичные зерна в клубочках и в капсуле, а также зернистое в стенках артериол, C1q комплимент: отрицательно. Каппа: отрицательно в клубочках, единичные очаги в интерстиции. Лямбда: отрицательно в клубочках, единичные очаги в интерстиции. Электронномикроскопически: толщина и структура базальных мембран в пределах нормы, депозитов не обнаружено. Имеются протяженные очаги распластывания малых отростков подоцитов, пролиферация мезангиальных клеток отсутствует. Результаты были интерпретированы как очаговое распластывание малых отростков подоцитов, а также тубулопатия неясного генеза. Особое внимание в клинической картине на себя обращало постепенное нарастание протеинурии, артериальной гипертензии на фоне снижения фильтрационной функции почек и канальцевой дисфункции. Подобная двойственность клинических проявлений препятствовала пониманию сути патологического процесса в почках, и не позволяла в полной мере проводить медикаментозную терапию, отвечающую патогенетическим и этиологическим принципам. Указание в анамнезе на длительный прием фитопрепаратов позволило предположить токсическое воздействие метаболитов кумарина на функциональное состояние почек, однако в доступной литературе нет прямых указаний на прямое нефротоксическое действие кумарина. Исследователи ограничивают область токсических влияний кумарина и его метаболитов на функцию печени и гемостаза. Действительно, в рассматриваемом клиническом примере отмечаются как нарушения гемостаза, характеризующиеся гипокоагуляцией, так и печеночная дисфункция. Однако по данным нефробиопсии отмечаются признаки токсического процесса на уровне канальцев почки, характеризующегося резко выраженной гидропической дистрофией эпителия канальцев вплоть до вакуолизации, слабым диффузным и мелкоочаговым фиброзом интерстиция. Эти изменения соотносятся с изменениями клубочков, характеризующимися выраженной интракапиллярной гиперклеточностью и пролиферацией базальных мембран, сегментарным расширением парамезангиальных зон, наличием очагов распластывания малых отростков подоцитов.
Таким образом, впервые в литературе описан случай прямого нефротоксического воздействия кумарина и его метаболитов. Повреждение канальцевого эпителия почек метаболитами кумарина обуславливается во многом изначальным повреждением гломерулярной базальной мембраны, а также дисморфизмом подоцитов, что обуславливает повышенную готовность канальцевого эпителия к повреждению на фоне усиления процессов реабсорбции в связи с дефектами гломерулярной базальной мембраны и подоцитов. В свою очередь, низкая молекулярная масса кумарина и его метаболитов позволяет свободно проникать через гломерулярный фильтр, что, в условиях повреждения базальной мембраны и подоцитов, приводит к критическому повышению его в первичной моче и обуславливает токсическое действие на уровне канальцев почки.
Литература
1. Ермоленко, В.М. Острая почечная недостаточность / В.М. Ермоленко, А.Ю. Николаев – М.: Гэотар-Медиа, 2010. – 400 с.
2. Angell, M. Alternative medicine – the risks of untested and unregulated remedies / M. Angell, J.P. Kassirer // N. Engl. J. Med. – 1998. – V.339. – P.839-841.
3. Fugh-Berman, A. Herb-drug interactions / A. Fugh-Berman // Lancet. – 2000. – V.355. – P.134-138.
4. Recent patterns of medication use in the ambulatory adult population of the United States: the Spone survey / D.W. Kaufman, J.P. Kelly, L. Rosenberg et al. // JAMA. – 2002. –V.287. – P.337-344.
5. Screening methods for drugs and heavy metals in Chinese patent medicines / A. Au, R. Ko, F. Boo et al. // Bull. Environ. Contam. Toxicol. – 2000. – V.5. – P.112-119.
6. Chopra, A. Ayurvedic medicine: core concept, therapeutic principles, and current relevance/ A. Chopra, V. Doiphode. // Med. Clin. North. Am. – 2002. – V.86. – P.75-89.
7. Ernst, E. Heavy metals in traditional Indian remedies / E. Ernst // Eur. J. Clin. Pharmacol. – 2002. – V.57. – P.891-896.
8. The use and safety of non-allopathic Indian medicines / N. Gogtay, H. Bhatt, S. Dalvi, N. Kshirsagar // Drug Saf. – 2002. – V.25. – P.1005-1019.
9. Indian herbal remedies for diabetes as a cause of lead poisoning / R.W. Keen, A.C. Deacon, H.T. Delves et al. // Postgraduate Medical Journal. – 1994. – V.70. – P.113-114.
10. Ko, R.J. Adulterants in Asian patent medicines / R.J. Ko // N. Engl. J. Med. – 1998. – V.339. – P.847.
11. Arlt, V. Aristolochic acid as a probable human cancer hazard in herbal remedies: a review / V. Arlt, M. Stiborova, H. Schmeiser // Mutagenesis. – 2002. – V.17. – P.265-277.
12. Trends in alternative medicine use in the United States, 1990-1997: results of a follow-up national survey / D.M. Eisenberg, R.B. Davis, S.L. Ettner et al. // JAMA. – 1998. – V.280. – P.1569-1575.
13. Ernst, E. Adulteration of Chinese herbal medicines with synthetic drugs: a systematic review / E. Ernst // J. Intern. Med. – 2002. – V.252. – P.107-113.
14. Foote, J. Medicinal herb use and the renal patient / J. Foote, B. Cohen // J. of Renal Nutrition. – 1998. – V.8. – P.40-42.
15. International Agency for Research on Cancer (IARC). Some traditional herbal medicines, some mycotoxins, nafhtalene and styrene. In IARC Monographs on the Evaluation of Carcinogenic Risks of Chemicals to Humans. Lyon. France: IARC, 2002. – Р.82.
16. Herbs and the kidney/ C. Isnard Bagnis, G. Deray, A. Baumelou et al. // Am. J. Kidney Dis. – 2004. – V.44. – №1. – P.1-11.
17. Morris L. Side-effects of coumarin / L. Morris, P.D. Welsby // Postgrad. Med. J. – 1995. – №71. – P.701-702.
18. British Herbal Pharmacopoeia. – 1996. – 212 p.
19. Advances in research on chemical constituents and pharmacological activities of Agrimonia pilosa / G. Hong, Y.H. Dai, P.X. Liu et al.// Pharm. Care and Research. – 2008. – V.8. – № 5. – P.362-366.
20. Карташова, Г.С. Содержание дубильных веществ в Agrimonia pilosa Ledeb. / Г.С. Карташова, И.В. Гравель, Е.Г. Таран // Растительные ресурсы. – 1991. – Т.27. – №1. – С.139-143.
21. Wei, Y. Isolation of hyperoside and luteolin-glucoside from agrimonia pilosa ledeb using stepwise elution by high-speed countercurrent chromatography / Y. Wei, Y. Ito // J. of Liquid Chromatography and Related Technologies. – 2007. – V.30. – №9-10. – P.1465–1473.
22. Separation and determination of flavonoids in Agrimonia pilosa Ledeb. by capillary electrophoresis with electrochemical detection / X. Xu, X. Qi, W. Wang, G. Chen // J. of Separation Science. – 2005. – V.28. – №7. – P.647-652.
23. Analysis of the volatile components of Agrimonla Pilosa Ledeb by gas chromatography-mass spectrometry / Y.W. Li, L.F. Huang, C. Liang et al. // J. of Central South University (Science and Technology). – 2007. – V.38. – №3. – P. 502-506.
24. Фитохимическое исследование растений флоры Сибири / Д.Л. Макарова, В.В. Величко, Н.Е. Ким и др.// Фармация. – 2008. – №3. – С.19-22.
25. 500 важнейших лекарственных растений / В.К. Лавренов, Г.В. Лавренова. – М., 2003. – 510 с. 26. Comparative metabolism and kinetics of coumarin in mice and rats / S.L. Born, A.M. Api, R.A. Ford et al. // Food Chem. Toxicol. – 2003. – №41. – P.247-258.
Статья опубликована в журнале «Вестник урологии». Номер №3/2013 стр. 30-39
Псориаз и современные методы его лечения
Псориаз (чешуйчатый лишай) — хроническое, весьма распространенное заболевание кожи, известное с давних времен. Распространенность его в различных странах колеблется от 0,1 до 3%. Однако эти цифры отражают лишь удельный
Псориаз (чешуйчатый лишай) — хроническое, весьма распространенное заболевание кожи, известное с давних времен. Распространенность его в различных странах колеблется от 0,1 до 3%. Однако эти цифры отражают лишь удельный вес псориаза у больных с другими дерматозами или частоту его встречаемости у пациентов с внутренними болезнями. Поскольку болезнь часто носит локализованный и неактивный характер, больные обычно не обращаются за помощью в медицинские учреждения, а следовательно, нигде не регистрируются.
Причина болезни остается неясной. Несмотря на огромное количество предлагаемых гипотез, ни одна не является общепризнанной. Четко установлена лишь роль генетических факторов — семейный показатель больных в несколько раз превышает популяционный. Есть указания на связь псориаза с антигенами HLA-cистемы — В13, В15, В16, В17, В27, В39, Dw11, DRW6, DR7, A1. Имеются данные о возможной патогенетической значимости генетических маркеров Lewis, MN, Ss, Duffy, Hp.
Основным патогенетическим звеном, вызывающим появление кожных высыпаний, являются повышенная митотическая активность и ускоренная пролиферация клеток эпидермиса, приводящая к тому, что клетки нижних слоев «выталкивают» вышележащие клетки, не дав им ороговеть. Этот процесс носит название паракератоза и сопровождается обильным шелушением. Большое значение в развитии псориатических поражений в коже играют местные иммунопатологические процессы, связанные с взаимодействием различных цитокинов — фактора некроза опухоли, интерферонов, интерлейкинов, а также лимфоцитов различных субпопуляций.
Пусковым моментом возникновения болезни часто является сильный стресс — этот фактор присутствует в анамнезе большинства больных. К другим триггерным факторам можно отнести травмы кожи, применение медикаментов, злоупотребление алкоголем, инфекции.
Многочисленные нарушения в эпидермисе, дерме и во всех системах организма тесно связаны и не могут по отдельности объяснить механизм развития болезни.
Общепринятой классификации псориаза нет. Традиционно наряду с обычным (вульгарным) псориазом выделяют эритродермическую, артропатическую, пустулезную, экссудативную, каплевидную, ладонно-подошвенную формы.
Обычный псориаз клинически проявляется образованием плоских папул, четко отграниченных от здоровой кожи. Папулы розовато-красного цвета, покрыты рыхлыми серебристо-белыми чешуйками. С диагностической точки зрения интересна группа признаков, возникающих при поскабливании папул и называемых псориатической триадой. Сначала появляется феномен «стеаринового пятна», характеризующийся усилением шелушения при поскабливании, что придает поверхности папул сходство с каплей стеарина. После удаления чешуек наблюдается феномен «терминальной пленки», проявляющийся в виде влажной блестящей поверхности элементов. Вслед за этим при дальнейшем поскабливании отмечается феномен «кровяной росы» — в виде точечных, несливающихся капелек крови.
Высыпания могут располагаться на любом участке кожного покрова, но преимущественно локализуются на коже коленных и локтевых суставов и волосистой части головы, с поражения которой очень часто заболевание начинается. Для псориатических папул характерна склонность к периферическому росту и слиянию в бляшки различных размеров и очертаний. Бляшки могут быть изолированными, небольшими или крупными, занимающими обширные участки кожных покровов.
При экссудативном псориазе меняется характер шелушения — чешуйки становятся желтовато-сероватыми, склеиваются с образованием корочек, плотно прилегающих к коже. Сами высыпания более яркие и отечные, чем при обычном псориазе.
Псориаз ладоней и подошв может наблюдаться в виде изолированного поражения или сочетаться с поражениями других локализаций. Проявляется он в виде типичных папуло-бляшечных элементов, а также гиперкератотических, мозолеподобных очагов с болезненными трещинами или пустулезных высыпаний.
Практически всегда при псориазе поражаются ногтевые пластинки. Наиболее патогномоничным считается появление на ногтевых пластинках точечных вдавлений, придающих ногтевой пластинке сходство с наперстком. Также могут отмечаться разрыхление ногтей, ломкость краев, изменение окраски, поперечные и продольные борозды, деформации, утолщение, подногтевой гиперкератоз.
Псориатическая эритродермия является одной из наиболее тяжелых форм псориаза. Она может развиваться за счет постепенного прогрессирования псориатического процесса и слияния бляшек, но чаще возникает под влиянием нерационального лечения. При эритродермии вся кожа приобретает ярко-красный цвет, становится отечной, инфильтрированной, отмечается обильное шелушение. Больных беспокоит сильный зуд, ухудшается общее состояние.
Рентгенологически различные изменения костно-суставного аппарата наблюдаются у большинства больных без клинических признаков поражения суставов. К таким изменениям относят околосуставной остеопороз, сужение суставных щелей, остеофиты, кистозные просветления костной ткани. Диапазон клинических проявлений может варьировать от незначительных артралгий до развития инвалидизирующего анкилозирующего артроза. Клинически обнаруживаются припухлость суставов, покраснение кожи в зоне пораженных суставов, болезненность, ограничение подвижности, деформации суставов, анкилозы, мутиляции.
Пустулезный псориаз проявляется в виде генерализованных или ограниченных высыпаний, локализованных преимущественно на коже ладоней и подошв. Хотя ведущим симптомом этой формы псориаза считается возникновение на коже пустул, считающихся в дерматологии проявлением гнойничковой инфекции, содержимое этих пузырьков обычно стерильно.
Каплевидный псориаз чаще развивается у детей и сопровождается внезапным высыпанием рассеянных по всему кожному покрову мелких папулезных элементов.
Псориаз наблюдается примерно с одинаковой частотой у мужчин и женщин. У большинства пациентов заболевание начинает развиваться до 30 лет. У многих больных отмечается связь обострений с временем года: чаще заболевание обостряется в холодный период (зимняя форма), гораздо реже — летом (летняя форма). В дальнейшем эта зависимость может меняться.
В течении псориаза различают 3 стадии: прогрессирующую, стационарную и регрессирующую. Для прогрессирующей стадии характерны рост по периферии и появление новых высыпаний, особенно на местах прежних высыпаний (изоморфная реакция Кебнера). В регрессирующей стадии наблюдается уменьшение либо исчезновение инфильтрации по окружности или в центре бляшек.
Вульгарный псориаз дифференцируют от парапсориаза, вторичного сифилиса, красного плоского лишая, дискоидной красной волчанки, себорейной экземы. Сложности возникают при дифференциальной диагностике ладонно-подошвенного и артропатического псориаза.
При вульгарном псориазе прогноз для жизни благоприятный. При эритродермии, артропатическом и генерализованном пустулезном псориазе возможны инвалидизация и даже летальный исход из-за истощения и развития тяжелых инфекций.
Неопределенным прогноз остается в отношении продолжительности заболевания, длительности ремиссии и обострений. Высыпания могут существовать длительно, многие годы, но чаще обострения чередуются с периодами улучшения и клинического выздоровления. У значительной части больных, в особенности не подвергавшихся интенсивному системному лечению, возможны многолетние, самопроизвольные периоды клинического выздоровления.
Нерациональное лечение, самолечение, обращение к «целителям» ухудшают течение болезни, приводят к обострению и распространению кожных высыпаний. Именно поэтому основная цель данной статьи — дать краткую характеристику современным методам лечения этой болезни.
Сегодня существует огромное количество методов лечения псориаза, в терапии этого заболевания используются тысячи различных препаратов. Ноэто лишь означает, что ни один из методов не дает гарантированного эффекта и не позволяет вылечить болезнь окончательно. Более того, вопрос об излечении и не ставится — современная терапия в состоянии лишь свести к минимуму кожные проявления, не затрагивая многих неизвестных на сегодня патогенетических факторов.
Лечение псориаза проводится с учетом формы, стадии, степени распространенности высыпаний, общего состояния организма. Как правило, лечение комплексное, предусматривающее сочетание наружных и системных препаратов.
Большое значение при лечении имеют мотивация пациента, семейные обстоятельства, социальное положение, образ жизни, злоупотребление алкоголем.
Способы лечения можно разделить на следующие направления: наружная терапия, системная терапия, физиотерапия, климатотерапия, нетрадиционные и народные методы.
Наружная терапия
Терапия препаратами наружного действия имеет при псориазе важнейшее значение. В легких случаях лечение начинают с местных мероприятий и ими ограничиваются. Как правило, препараты для местного применения реже оказывают какие-либо побочные действия, но по эффективности уступают системной терапии.
В прогрессирующей стадии наружное лечение проводят с большой осторожностью, чтобы не вызвать ухудшения состояния кожи. Чем интенсивнее воспаление, тем меньшей должна быть концентрация мазей. Обычно на этой стадии при лечении псориаза ограничиваются кремом «Унна», 0,5–2% салициловой мазью, травяными ваннами.
На стационарной и регрессирующей стадии показаны более активные препараты — 5–10% нафталановая мазь, 2–10% мазь АСД, 2–5% салициловая мазь, 2–5% серно-дегтярная мазь, а также многие другие способы терапии.
В современных условиях при выборе способа терапии или конкретного препарата врач должен руководствоваться официальными протоколами и формулярами, разработанными руководящими органами здравоохранения. В Федеральном руководстве по использованию лекарственных средств (выпуск IV) для местного лечения больных псориазом предлагаются стероидные лекарственные средства, салициловая мазь, препараты дегтя и кальципотриол.
Исходя из «Методических материалов по диагностике и лечению наиболее распространенных инфекций, передаваемых половым путем, и заболеваний кожи», разработанных ЦНИКВИ в 2001 г., в качестве наружной терапии используют 1–2% салициловую мазь, мази с содержанием дегтя 5–10%, нафталана 5–10%, витамина Д3, а также кортикостероидные мази (бетаметазон с салициловой кислотой, мометазон) и аэрозоль цинка пиритионата. В «Протоколах ведения больных», разработанных учеными ЦНИКВИ в 2003 г., рекомендуются те же препараты.
Остановимся в основном на указанных в руководствах препаратах.
Гидратитрующие средства. Смягчают шелушащуюся поверхность псориатических элементов, уменьшают стягивание кожи, улучшают эластичность. Используют кремы на основе ланолина с витаминами, крем «Унна». По данным литературы, даже после такого легкого воздействия клинические эффекты (снижение зуда, эритемы и шелушения) достигаются у трети больных.
Препараты салициловой кислоты. Обычно используют мази с концентрацией от 0,5 до 5% салициловой кислоты. Она обладает антисептическим, противовоспалительным, кератопластическим и кератолитическим действием, может применяться в комбинации с дегтем и кортикостероидами. Салициловая мазь размягчает шелушащиеся слои псориатических элементов, а также усиливает действие местных стероидов путем усиления их всасывания, поэтому часто используется в комбинации с ними. Сама салициловая кислота легко проникает в кожу и затем в кровь. Поэтому ее не применяют на обширных поверхностях и в концентрации больше 2%, а у детей даже 2-процентную мазь накладывают только на ограниченных участках кожи. Непереносимость встречается редко, однако салициловая кислота может вызывать в качестве побочного эффекта усиление воспаления кожи.
Дегтярные препараты. Применяются издавна в виде 5–15% мазей и паст, часто в сочетании с другими местными препаратами. В России используются мази с древесным дегтем (обычно березовым), в некоторых зарубежных странах — с каменноугольным. Последний более активен, но, как считают наши ученые, обладает канцерогенными свойствами, хотя многочисленные публикации и зарубежный опыт не подтверждают этого. Деготь превосходит салициловую кислоту по активности, обладает противовоспалительными, кератопластическими и антиэксфолиативными свойствами. Его применение при псориазе обусловлено, кроме того, влиянием на клеточную пролиферацию. Применение дегтярных препаратов ограничено из-за неприятного запаха, их нельзя накладывать на лицо. Комбинации дегтя с цинком или салициловой кислотой не обладают значительными преимуществами перед монокомпонентными препаратами дегтя. Способность дегтя повышать фоточувствительность используется для комбинированной терапии в сочетании с ультрафиолетовым облучением. Не следует применять препараты дегтя длительно и в повышенной концентрации, так как это может привести к всасыванию и системному действию (поражение почек, общая интоксикация, паралич). При назначении препаратов дегтя следует учитывать его фотосенсибилизирующее действие и риск ухудшения функции почек у лиц с нефрологическими болезнями.
Для мытья головы используют шампуни с дегтем (фридерм-тар, Т/гель).
Нефть нафталанская. Смесь углеводородов и смол, содержит серу, фенол, магний и много других веществ. Препараты нафталанской нефти обладают противовоспалительными, рассасывающими, противозудными, антисептическими, отшелушивающими и репарационными свойствами. Для лечения псориаза применяются 10–30% нафталановые мази и пасты. Часто нафталанская нефть используется в комбинации с серой, ихтиолом, борной кислотой, цинковой пастой.
Местная терапия ретиноидами. Первый эффективный местно применяемый ретиноид, разрешенный к употреблению как средство для лечения псориаза, — тазаротен. В России этот препарат пока не зарегистрирован. Он представляет собой желе на водной основе и выпускается в концентрации 0,05 и 0,1%. По эффективности он сравним с сильнодействующими ГКС. Из побочных эффектов отмечаются зуд и раздражение кожи. Одним из преимуществ этого препарата является более продолжительная по сравнению с ГКС ремиссия. Так, по данным J. Koo, через 3 мес после лечения рецидив наблюдали только у 185 больных (после флуоцинонида — у 55%). В работе A. Marchetti показаны фармакоэкономические преимущества тазаротена в виде 0,1% геля в сравнении с мазью флуоцинонида (местный ГКС) и кальципотриена (разновидность витамина Д3 для местного использования).
Гидрантроны. В первой половине XX в. применялись мази со смесью естественных дериватов антрацена — хризаробином, который получали из стволов бразильского дерева Vonacopua araroba семейства бобовых.
В настоящее время в Европе и США используются синтетические гидроксиантроны — дитранол, антралин, цигнолин, антраробин.
Дитранол — аналог естественного хризаробина, оказывает цитотоксическое и цитостатическое действие, приводит к снижению активности окислительных и гликолитических процессов в эпидермисе. В результате уменьшаются количество митозов в эпидермисе, а также гиперкератоз и паракератоз. К сожалению, дитранол обладает выраженным местно-раздражающим действием, и при попадании на здоровую кожу могут возникать ожоги. С другой стороны, дитранол очень эффективен и не вызывает системных побочных эффектов. Несколько лет назад в Европе появились препараты, которые высвобождают дитранол только при температуре кожи человека (миканол). В результате ослабляется окрашивание кожи. Сегодня дитранол применяют в достаточно высоких концентрациях (>1%), нанося его на 5–30 минут. Этот способ не уступает по эффективности применению препарата в низких концентрациях на ночь. По данным литературы, средняя ремиссия при лечении дитранолом составляет 4 – 6 мес.
Российские специалисты редко используют препараты этой группы, в России они не производятся и за рубежом не закупаются. Ранее предлагались несколько препаратов этой группы — цигнодерм, дитрастик, псоракс. Они выпускаются в виде стержня, наподобие губной помады. Добавление парафина позволяет наносить препараты точно на область поражения, что особенно удобно при лечении ограниченных, застарелых очагов.
К препаратам этой группы можно отнести антралин, который применяется в европейских и американских лечебных центрах. Препарат тормозит синтез ДНК ядра и митохондрий, угнетает метаболизм в тканях, что приводит к снижению пролиферации. При использовании сильно окрашивает контактируемые поверхности, может вызывать раздражения и ожоги.
Производные иприта.
К ним относятся псориазин и антипсориатикум. В их состав входят вещества кожно-нарывного действия — иприт и трихлорэтиламин. Лечение этими препаратами проводят с большой осторожностью, применяя сначала мази с небольшой концентрацией на небольшие очаги поражения 1 раз в день. Затем при хорошей переносимости концентрацию, площадь и кратность при использовании увеличивают. Лечение осуществляют под тщательным врачебным контролем, проводя еженедельные тесты крови и мочи. Сейчас данные препараты практически не применяются, однако они весьма эффективны в стационарной стадии болезни.
Цинка пиритионат. Активное вещество, выпускаемое в виде аэрозолей, кремов и шампуней под торговым названием «Скин-кап». Обладает противомикробным, противогрибковым, а также антипролиферативным действием — подавляет патологический рост клеток эпидермиса, находящихся в состоянии гиперпролиферации. Последнее свойство определяет эффективность препарата при псориазе. Препарат снимает воспаление, уменьшает инфильтрацию и шелушение псориатических элементов. Лечение проводят в среднем в течение месяца. Для терапии больных с поражениями волосистой части головы используют аэрозоль и шампунь, при поражениях кожи — аэрозоль и крем. Препарат наносят 2 раза в сутки, шампунь применяют 3 раза в неделю. В России начиная с 1995 г. проводилось изучение клинической эффективности и переносимости всех лекарственных форм цинка пиритионата. По заключению ведущих дерматологических центров — ЦНИКВИ, РГМУ, ММА, ВМА — эффективность препарата при лечении больных псориазом достигает 85–90%. Исходя из данных, опубликованных в периодической печати ведущими специалистами этих и других центров, клинического излечения удается добиться к концу 3–4 нед лечения. Эффект развивается постепенно, но очень важно, что результаты лечения очевидны уже к концу первой недели с момента начала применения препарата — резко снижается зуд, устраняется шелушение, бледнеет эритема. Такое быстрое достижение клинического эффекта приводит, соответственно, к быстрому улучшению качества жизни пациентов. Препарат хорошо переносится. Разрешен для применения с 3- летнего возраста.
Мази с витамином Д3. С 1987 г. при местном лечении используется синтетический препарат витамина Д3 — кальципотриол. Многочисленными экспериментальными исследованиями показано, что кальципотриол вызывает торможение пролиферации кератиноцитов, ускоряет их морфологическую дифференциацию, воздействует на факторы иммунной системы кожи, регулирующие пролиферацию клеток, обладает противовоспалительными свойствами. На российском рынке представлены 3 препарата данной группы от различных производителей. Препараты наносят на пораженные участки кожи 1-2 раза в сутки. Эффективность мазей с Д3 примерно соответствует эффекту кортикостероидных мазей I, II классов, а по данным J. Koo — даже III класса. При применении этих мазей выраженный клинический эффект наступает у большинства больных (до 95%). Однако для достижения хорошего эффекта может понадобиться достаточно много времени (от 1 мес до 1 г.), а площадь поражения не должна превышать 40%. И. В. Хамаганова сообщает о положительном опыте применения кальципотриола у детей. Препарат наносили 2 раза в день, выраженный эффект наблюдался к концу четвертой недели лечения. Побочных эффектов не выявлено. О таких же результатах лечения при использовании кальципотриола у взрослых сообщает В. А. Самсонов.
Иногда при использовании кальципотриола могут наблюдаться раздражение кожи, дерматит, фотосенсибилизация, обострение псориатического процесса, гиперкальциемия. Однако кальципотриол не вызывает побочных эффектов, характерных для стероидов, и иногда дает более стойкий эффект, чем мази с ГКС. Хотя, по данным того же J. Koo, рецидивы возникают у более 50% больных, при этом средняя продолжительность ремиссии не превышает 1,5 мес.
Более выраженных эффектов достигают при сочетанном применении кальципотриола с любыми формами фототерапии, а также с системной терапией.
Кортикостероидные препараты. Применяются в медицинской практике в качестве наружных средств с 1952 г., когда Sulzberger впервые показал эффективность наружного применения стероидов. На сегодняшний день на российском фармацевтическом рынке зарегистрированы около 50 глюкокортикостероидных средств для наружного применения. Это, несомненно, затрудняет выбор врача, который должен иметь информацию обо всех препаратах. Специальное анкетирование, проведенное Н. Г. Кочергиным среди дерматологов, показало, что при выборе средств для наружной терапии врачи исходят из следующих данных: активности кожного процесса, локализации высыпаний, возраста больного, эффективности рекламы и стоимости препарата в аптеке. К наиболее часто назначаемым при псориазе ГКС, по данным того же опроса, относятся комбинированные препараты (флуметазона пивалат с салициловой кислотой), мометазона фуроат или бетаметазона дипропионат.
Терапевтический эффект наружных ГКС обусловлен целым рядом потенциально благоприятных эффектов:
Изменение структуры ГКС отражалось на их свойствах, активности. Так появилась достаточно обширная группа препаратов, различающихся по своему химическому строению и активности. Гидрокортизона ацетат сегодня при псориазе практически не применяется, его используют в клинических исследованиях для сравнения со вновь получаемыми препаратами. Например, считается, что если активность гидрокортизона принять за единицу, то активность триамцинолона ацетонида составит 21 единицу, а бетаметазона — 24 единицы. Из препаратов второго класса при псориазе чаще используется флуметазона пивалат в комбинации с салициловой кислотой, а наиболее современными являются нефторированные ГКС. В связи с минимальным риском возникновения побочных явлений мази и кремы с аклометазоном разрешены для применения на чувствительных участках (лицо, кожные складки), лечения детей и пожилых людей, при нанесении на обширные участки кожи.
Среди препаратов третьего класса можно выделить группу фторированных ГКС — флуоцинолона ацетонид, триамцинолона ацетонид, бетаметазона валерат и дипропионат. Фармакоэкономический анализ применения этих препаратов (правда, не при псориазе), заключающийся в изучении соотношения «цена/безопасность/эффективность», по данным В. А. Аковбяна, выявил благоприятные показатели у бетаметазона валерата — быстрое развитие терапевтического эффекта, более низкая стоимость курса лечения.
При лечении псориаза начинать следует с более легких препаратов — гидрокортизона, преднизолона, аклометазона, а при повторных обострениях и неэффективности используемых препаратов давать более сильные. Однако среди американских дерматологов популярна следующая тактика: вначале применяется сильный ГКС для достижения быстрого эффекта, а потом пациента переводят на умеренный или слабый препарат для проведения поддерживающей терапии. В любом случае сильные препараты используют короткими курсами и лишь на ограниченные участки, так как при их назначении чаще развиваются побочные эффекты.
Помимо указанной классификации, препараты подразделяют на фторированные, дифторированные и нефторированные средства разных поколений. Нефторированные ГКС первого поколения (гидрокортизона ацетат) по сравнению с фторированными, как правило, менее эффективны, но более безопасны в отношении побочных реакций. Сейчас проблема низкой эффективности нефторированных ГКС уже решена — созданы нефторированные препараты четвертого поколения, сравнимые по силе с фторированными, а по безопасности — с гидрокортизона ацетатом. Это, в частности, гидрокортизона бутират, мометазона фуроат, метилпреднизолона ацепонат. Проблема усиления действия препарата решается не путем галогенизации, а благодаря этерификации. Кроме усиления действия это позволяет использовать этерифицированные препараты 1 раз в сутки. К примеру, гидрокортизона бутират имеет следующие фармакодинамические свойства: торможение миграции лейкоцитов и лимфоцитов в область воспаления, угнетение протеолитической активности тканевых кининов, задержка роста фибробластов, предупреждение развития соединительной ткани в очаге воспаления. Именно нефторированные ГКС четвертого поколения являются сегодня предпочтительными для местного применения при псориазе.
Стандартные побочные эффекты при применении местных стероидов — это развитие атрофии кожи, гипертрихоза, телеангиэктазий, гнойничковых инфекций, системное действие с влиянием на гипоталамо-гипофизарно-надпочечниковую систему. В современных нефторированных препаратах, упомянутых выше, эти побочные эффекты сведены к минимуму.
Фармацевтические компании стараются разнообразить спектр лекарственных форм и выпускают ГКС в виде мазей, кремов, лосьонов. Жирная мазь, создавая пленку на поверхности очага поражения, вызывает более эффективное рассасывание инфильтрации, чем другие лекарственные формы. Крем лучше купирует островоспалительные явления, увлажняет, охлаждает кожу. Безжировая основа лосьона обеспечивает его легкое распределение по поверхности волосистой части головы без склеивания волос.
По литературным данным, при использовании, например, мометазона в течение 3 нед положительного терапевтического эффекта (уменьшения количества высыпаний на 60–80%) удается добиться почти у 80% больных. По данным В. Ю. Уджуху, наиболее выгодного соотношения «эффективность/безопасность» можно достичь при использовании гидрокортизона бутирата. Выраженный клинический эффект при применении этого препарата сочетается с хорошей переносимостью — ни у одного из прошедших курс лечения больных авторы не наблюдали побочных реакций, даже при нанесении на лицо. При длительном использовании других ГКС приходилось останавливать лечение из-за развития побочных эффектов. По данным B. Bianchi и Н. Г. Кочергина, сравнение результатов клинического применения мометазона фуората и метилпреднизолона ацепоната показало одинаковую эффективность этих лекарственных средств при наружном применении. Ряд авторов (Е. Р. Аравийская, Е. В. Соколовский) предлагают этапную кортикостероидную терапию псориаза. Рекомендуется начинать наружную терапию с комбинированных препаратов, содержащих ГКС (например, бетаметазон и салициловую кислоту). Средняя продолжительность такого лечения — около 3 нед. В дальнейшем происходит переход на чистый ГКС, желательно третьего класса (например, гидрокортизона бутират или мометазона фуроат).
Больных привлекают простота использования стероидных препаратов, возможность достаточно быстро снять клиническую симптоматику заболевания, доступность, отсутствие запаха. Кроме того, эти лекарственные средства не оставляют жирных пятен на одежде. Однако их применение должно быть кратковременным, во избежание ухудшения течения болезни. При длительном применении стероидных мазей развивается привыкание. Резкая отмена кортикостероидов может вызвать обострение кожного процесса. В литературе указывается разная длительность ремиссии после местного лечения кортикостероидами. Большинство работ свидетельствует о непродолжительной ремиссии — от 1 до 6 мес. Исследования R. Seville установили, что ГКС в комбинации с другими методами (в частности, с дитранолом) повышают эффективность лечения, но уменьшают длительность ремиссии. Пациентам нужно рекомендовать как можно дольше обходиться без применения кортикостероидных мазей. Во многих зарубежных источниках мази, содержащие глюкокортикостероидные гормоны, рекомендуют предпочтительно использовать на ограниченных открытых участках поверхности кожи — лицо, руки. Однако следует помнить об опасности развития на лице стероидного периорального дерматита или розацеа, особенно при применении фторированных ГКС.
При псориазе наиболее эффективны комбинации стероидных гормонов (чаще всего бетаметазона) с салициловой кислотой. Салициловая кислота благодаря своему кератолитическому и противомикробному действию дополняет дерматотропную активность стероидов.
На волосистую часть головы удобно наносить комбинированные лосьоны с кортикостероидами и салициловой кислотой. По данным отечественных авторов (Г. И. Суколин, В. А. Молочков, Н. С. Потекаев), эффективность комбинированных препаратов достигает 80 — 100%, при этом очищение кожи происходит очень быстро —в течение 3 нед.
Подводя итоги, следует сказать, что на практике врачу всегда необходимо решать, использовать ли только наружные методы лечения или назначать их в сочетании с какой-либо системной терапией в целях повышения эффективности лечения и удлинения ремиссии.
Ю. Н. Перламутров, доктор медицинских наук, профессор
А. М. Соловьев, кандидат медицинских наук
МГМСУ, Москва